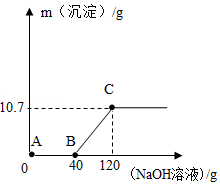
向盛有Fe2O3粉末的烧杯中加入过量的稀H2SO4,充分搅拌,粉末完全溶解;再向所得溶液中逐滴加入NaOH溶液,生成沉淀与加入NaOH溶液之间的质量关系如图所示。请回答下列问题:
(1)写出AB段内反应的化学方程式: 。
(2)加入NaOH溶液40g时溶液中存在的溶质是 (写化学式)。
(3)计算氢氧化钠溶液中溶质的质量分数。(要求写出计算过程)
某化学兴趣小组在学习酸碱中和反应实验时,进行了如下探究。
I.探究酸和碱能否发生反应
甲同学向盛有少量KOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由 色变成无色。甲同学得出结论:酸和碱能发生反应。
请写出稀硫酸和氢氧化钾溶液反应的化学方程式 。
Ⅱ.探究酸和碱反应后溶液中溶质的成分
乙同学对探究I中甲同学实验后的无色溶液展开探究
[提出问题]试管中无色溶液的溶质除了酚酞还有什么?
[提出猜想](1)K2SO4:(2)K2SO4和
[设计实验]
|
方案 |
实验操作 |
实验现象及方程式 |
实验结论 |
|
方案1 |
向试管中加入少量碳酸钠,然后加入过量甲同学实验后的无色溶液 |
可观察到溶液中有 气泡 产生。化学反应方程式为 。 |
猜想(2)成立 |
|
方案2 |
用玻璃棒蘸取少量反应后的溶液滴在pH试纸上 |
|
|
|
方案3 |
用玻璃棒蘸取少量甲同学实验后的无色溶液,然后慢慢加NaOH溶液,并不断振荡试管 |
无明显现象,过一会发现 . |
[发散思维]为了验证猜想(2)成立,你认为还可以选择的物质是 (填选项)。
A.Ba(NO3)2 B.锌粒 C.Cu D.盐酸
如图是实验室制取气体时常用的装置,请回答下列问题。

(1)仪器①的名称是 ,仪器②的名称是 :
(2)实验室用氯酸钾和二氧化锰为原料制取氧气的气体发生装置应选 (填编号),化学反应方程式为 ;反应结束后,欲从剩余残渣中回收氯化钾,现有以下步骤:①蒸发结晶②过滤③洗涤、烘干④溶解,正确的操作顺序是 (填序号)
(3)用盛满水的G装置收集氧气时,气体应从 (填“a”或“b”)通入;
(4)实验室制取并收集一瓶干燥的CO2气体,选用的装置依次是 (填编号)
(5)二氧化硫气体是一种有刺激性气味的有毒气体,实验室制取SO2气体时需进行尾气处理,应选择的装置是 (填编号)。
我国南海蕴藏着丰富的油气资源。工业上可用甲烷(CH4)裂解制取高质量炭黑和氢气,反应的化学方程式为:CH4 C+2H2,现将32吨甲烷裂解,可制得氢气的质量是多少?
小红将30g氯酸钾和二氧化锰的固体混合物加热制取氧气,待反应完全后,将试管冷却、称量,得到固体的总质量为20.4g,请计算:
(1)生成氧气的质量是多少克?
(2)原混合物中氯酸钾的质量是多少?
(3)混合物中二氧化锰的质量是多少?(写出计算过程)
已知KNO3在20℃时的溶解度是31.6g,求此温度下将15.8g KNO3固体溶于水配成饱和溶液,需加水 克,所得溶液的溶质质量分数是 。