经过一年的学习,同学们认识了很多化学物质,它们在一定条件下可以转化或者相互反应。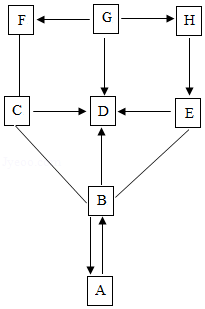
如图所示,A~H是初中化学所学的八种不同物质。“﹣”表示相连两物质之间能发生反应,“→”表示一种物质能转化成另一种物质。(部分反应物、生成物、反应条件已略去)
(1)已知A物质俗称纯碱,它的另一个俗称是 。
(2)已知H是磁铁矿的主要成分Fe3O4,F是黑色固体,则F是 O ,G→H的化学反应基本类型是 。
(3)D是 。
(4)写出B和C反应的化学方程式: 。
(5)写出A→B反应的化学方程式: 。
水是常用溶剂,某同学进行如图实验。

(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是 。
(2)实验可知,溶质状态可以是 。
(3)实验结束后,用洗涤剂洗净B试管,原理是 。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知:2KMnO4+16HCl(浓)═2KCl+2X+5Cl2↑+8H2O,X的化学式为 。
(5)询问老师得知用2NaOH+Cl2═NaCl+NaClO+H2O可处理Cl2。根据化学方程式计算,处理0.142g Cl2至少需NaOH的质量是多少?
嘌呤是合成DNA的主要物质,广泛存在于细胞核中,嘌呤的化学式为C5H4N4,在人体内会被氧化成尿酸,血液中尿酸含量过高容易引起痛风。
(1)嘌呤的相对分子质量为 。
(2)嘌呤中碳元素和氢元素的质量比为 。
按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管。环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。
(1)纤维素是一种 (选填“有机物”或“无机物”)。
(2)纤维素分子中,氢、氧原子的个数比为 。
(3)计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
|
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

氕、氘、氚是氢的三种同位素原子,它们的原子结构模型如图所示,相关信息如表。试回答
|
名称 |
符号 |
相对原子质量 |
|
氕 |
H |
1 |
|
氘 |
D |
2 |
|
氚 |
T |
3 |
(1)原子结构模型中的“⊗”表示的粒子是 。
(2)超重水有一定的放射性。一个超重水分子由两个原子和一个氧原子构成,其化学式可表示为T2O,T2O中T的化合价为 。
(3)重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是多少?