用如图装置在相应条件下完成下列实验
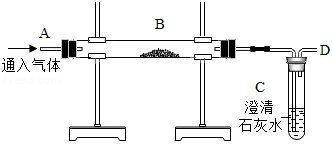
(1)探究燃烧条件:B盛木炭粉。
①由A处通N2一段时间后,加热B,B、C无明显变化。
②待B冷却至室温,由A处通入O2一段时间,B、C无明显变化。
③由A处继续通入O2,加热B,木炭粉燃烧,C中溶液变浑浊。
结论:由①、③可知燃烧需要 ;由②、③可知燃烧需要 。
(2)探究CO与金属氧化物反应:B盛金属氧化物。
I、模拟工业炼铁:A处通CO,B盛Fe2O3粉末,B处下方放酒精喷灯,D处放酒精灯。
实验:在A处通入CO时,应立即点燃 处(填“B”或“D”)酒精(喷)灯。在B处加热一段时间后可观察到的现象是 。
II、探究金属氧化物的组成:A处通CO,B盛金属氧化物,B处下方放酒精喷灯、D处放酒精灯。
已知:CuO、Fe3O4均为黑色物质,B中所盛粉末:CuO或Fe3O4或两者混合物。
实验:同Ⅰ操作、B中可观察到既有红色固体生成,又有黑色固体生成。
实验结论(定性):该黑色粉末为 。
定量分析:经测定反应前B重180克,完全反应后B重170.4克。将反应后B中固体全部加入到足量的稀硫酸中,完全反应后经过滤、洗涤、干燥,测得剩余固体12.8克。
实验结论(定量):m(CuO):m(Fe3O4)= (写最简整数比)。
2015年10月5日,中国籍科学家屠呦呦因发现治疗疟疾的新药物疗法而获得诺贝尔奖,青蒿素(化学式为C 15H 22O 5)是一种用于治疗疟疾的药物。青蒿素的发现挽救了全球特别是发展中国家数百万人的生命。
(1)青蒿素的相对分子质量是 。
(2)青蒿素中碳、氧元素的质量比为 。(填最简比)
某化学兴趣小组欲除去固体氯化钠中混有少量可溶性氯化镁和难溶性泥沙,设计如图所示实验方案,请参与实验并回答问题:

(1)步骤①、②中,操作X的名称是 。
(2)步骤②中,加入过量的NaOH溶液的目的是, 沉淀B的化学式是 。
(3)有同学认为该实验不完善,原因是 。
20℃时将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题。

①图1中,一定为饱和溶液的是 。
②图2中,甲、乙两溶液中溶质质量分数为甲 乙( 填"大于""等于""小于")。
③图3中,表示乙的溶解度曲线的是 ,P点表示的含义是 。
根据以下粒子结构示意图,回答问题:

①上述示意图中共包括 种元素。
②A、B、C、E中属于阴离子的是 (填离子符号)。
③若D表示某元素的原子,则m= 。
小型化工厂常以纯碱和大理石为主要原料,按以下工艺流程生产烧碱(NaOH)。

(1)物质C的化学式是 ,在步骤Ⅲ中要进行的分离操作是 。
(2)写出步骤Ⅰ的化学方程式: 。
(3)写出步骤Ⅲ的化学方程式: 。