请结合如图实验装置,回答问题:
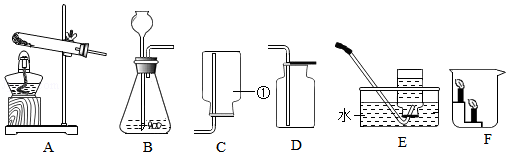
(1)写出标号①仪器的名称 。
(2)写出实验室用高锰酸钾制取氧气的化学方程式 ,可选择装置 (填序号)作为气体发生装置,但在该装置中还需要补充的是 。
(3)实验室常用大理石和稀盐酸制取二氧化碳气体,写出反应的化学方程式 ,收集气体应选用装置 (填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,可以观察到的现象是 ,说明二氧化碳具有 的物理性质。
X、Y、Z、W是初中化学常见的四种非金属元素.X的一种原子没有中子,Y的一种单质可用于制铅笔芯,Z是地壳中含量最高的元素,W2是空气中含量最高的单质.回答下列问题:
①Y的另一种单质是天然存在的最硬的物质,该单质的名称为 ,Z2﹣的离子结构示意图为 .
②X、Z、W三种元素可形成一种盐,该盐是一种常见的化肥,其化学式为 .
③实验室检验YZ2时发生反应的化学方程式为 .
④钠与Z形成的化合物Na2Z2常用作潜水艇中的供氧剂,因为Na2Z2与YZ2反应生成Na2YZ3和Z2,写出其反应的化学方程式 .
⑤X、Y、W三种元素可按质量比2:6:7形成一种的火箭燃料偏二甲肼,其相对分子质量为60,偏二甲肼在空气中完全燃烧的产物均无污染,其化学方程式为
.
课堂上老师对探究干电池原理的实验进行如下改进。
图甲:把一块锌片和一根碳棒同时插入盛有稀硫酸的U型管中;
图乙:用导线将锌片和碳棒连接起来插入盛有稀硫酸的U型管中,并在导线中间连接一只灵敏电流计。
请按要求回答问题:
(1)甲主要的能量转化形式是 。
(2)乙观察到与甲不同的现象是 、 。
(3)配制所需硫酸:现有98%的浓硫酸18g(体积为9.8mL),可将其配成24.5%的硫酸溶液 g,配制的具体操作过程是 。
(4)取(3)所配24.5%的硫酸溶液20g,向其中滴加25%的Ba(OH)2溶液至恰好完全反应。
①请计算产生沉淀的质量 g,写出必要的计算过程。
②沉淀过滤后水的质量是 g。

空气是宝贵的自然资源,其组成如表
|
空气组成 |
X |
O2 |
Y |
CO2 |
其它 |
|
体积分数 |
78% |
21% |
0.934% |
0.034% |
0.002% |
如图是空气等为原料合成尿素[CO(NH2)2]的流程(部分产物略去)。请按要求回答相关问题:
(1)X的分子式是 ,Y气体名称是 。
(2)煤的气化属于 变化。(选填“物理”或“化学”)。
(3)分离空气的常用方法有以下两种。
Ⅰ.将液态空气气化,首先分离出氮气。则沸点:X Y(选填“高于”、“等于”、“低于”)
Ⅱ.分子筛分离。分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:X O2(选填“大于”、“等于”、“小于”)。
(4)结合流程和所学知识可以预测:化学反应中发生物质变化的同时一定还伴随有 变化。(选填“状态”、“能量”、“原子”、“压强”)
(5)写出NH3合成尿素的化学方程式 。
(6)相同条件下气体体积之比等于分子之比,则空气中氮分子与氧分子总质量之比等于 。
已知:CO2和SO2既有相似性也有差异性。请回答相关问题:
|
气体 |
CO2 |
SO2 |
||
|
制备 |
石灰石与盐酸 |
Na2SO3与70%硫酸 |
||
|
相似性 |
溶解性 |
能溶于水 |
易溶于水 |
|
|
与澄清石灰水反应 |
二者都产生白色浑浊 |
|||
|
差异性 |
与KMnO4溶液 |
不反应 |
气体被吸收,溶液逐渐褪色 |
|
(1)化石燃料的气体产物中有CO2和SO2等物质,其中SO2是形成 的主要物质(填一污染名称)。
(2)制取CO2的化学方程式是 ,可用于收集CO2装置是 。(选填如图序号)。
(3)写出Na2SO3与70%硫酸反应的化学方程式 ,制备SO2发生装置用 。(选填如图序号)。
(4)将收集满SO2的试管倒扣在水中观察到的现象是 。
(5)结合已知信息,请你设计实验证明化石燃料燃烧的气体产物中有CO2(写出操作、试剂、现象、结论) 。
已知:铝在常温下能与O2反应,在铝表面形成一层氧化薄膜;Al2O3能溶于NaOH溶液。某课外小组对“铝与氯化铜溶液反应”进行如下探究。
①测得CuCl2溶液的pH<7;
②将铝片放入CuCl2溶液中,没有观察到现象;
③取出铝片用NaOH溶液浸泡一段时间,再取出铝片洗净后放入CuCl2溶液中,观察到铝表面产生无色气泡。
请回答下列问题:
(1)步骤①观察到CuCl2溶液呈 色,该溶液呈 性(选填“酸”、“碱”或“中”)。
(2)步骤③中还可能观察到的现象是 ,产生此现象的化学方程式是 。
(3)步骤②中没有现象的原因是 。
(4)小组对步骤③产生的气体提成以下猜想:
a.可能是Cl2; b.可能是O2; c.可能是 ;
小组讨论得出c成立,理由是 。