酸、碱、盐的溶解性表是学习化学的重要工具之一。下表是部分酸、碱、盐在水中的溶解性(20℃),请回答下列问题。
阴离子 阳离子 |
OH﹣ |
NO3﹣ |
CO32﹣ |
Cl﹣ |
K+ |
溶 |
溶 |
溶 |
溶 |
Ba2+ |
溶 |
溶 |
不 |
溶 |
Cu2+ |
不 |
溶 |
不 |
溶 |
(1)上述阴、阳离子形成不溶性碱的化学式为 ,形成复合肥料的化学式为 。
(2)KOH溶液和Ba(NO3)2溶液 (填“能”或“不能”)反应,理由是 。
(3)下列各组离子在水溶液中能大量共存的是 。
A.OH﹣、H+、Ba2+、NO3﹣
B.OH﹣、Ba2+、K+、Cl﹣
C.CO32﹣、K+、Ba2+、Cl﹣
D.CO32﹣、Cu2+、NO3﹣、K+
2012年6月,中国航天史上掀开极具突破性的一章:“神舟九号”实现了与“天宫一号”的载人交会对接。让我们一起解读“神九”:
(1)为航天员提供的“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、少量二氧化碳等气体。某同学对“人造空气”的分析如下:①氮气含量比空气低;②氮气没有任何作用,可不添加;③改成纯氧气更有益于航天员呼吸;④没有污染物。其中正确的是。
(2)“神九”载人飞船所用液态燃料是四氧化二氮和偏二甲肼的混合物。发射时,四氧化二氮和偏二甲肼发生剧烈反应如下: C2H8N2 + 2N2O4=2CO2 + 4H2O + 3X ,其中X的化学式为。
(3)为防止载人飞船在高温烘烤下表面被氧化,在载人飞船表面涂了一层纳米硅酸盐涂料。这种涂料应具有哪些性质?、。(至少答两点)
(4)三位宇航员所穿的航天服中有废气处理系统。先让废气进入一个装有活性炭的盒子除去臭气,这一过程利用了活性炭的性。再用氢氧化锂(LiOH)作吸收剂除去二氧化碳(氢氧化锂和氢氧化钙具有相似的化学性质),请写出该反应的化学方程式。
最近,由于气温下降使天然气需求量陡然增加,某城市有报道称天然气日缺20多万立方米,部分商户被停、限气。
(1)在家中厨房安装天然气泄漏报警器,正确位置应选择右图中的(填字母);如果漏气,下列应急措施不可行的有(填序号)。
A.关闭气源阀门 B.打开门窗 C.立即打开抽油烟机
(2)天然气在第一次通过管道输送到用户时,必须事先在管道内充满氮气,这样做的目的;天然气燃烧时,发生的反应方程式为。在使用天然气时常在其中加入少量有特殊气味的乙硫醇。加入乙硫醇的作用是。
(3)“可燃冰”又称天然气水合物(CH4·xH2O),它是在海底的高压、低温条件下形成的,1体积“可燃冰”可储藏100~200体积的甲烷。下列关于“可燃冰”的叙述中,错误的是。
A.“可燃冰”不是冰B.“可燃冰”的实质是水变成的固态油
C.“可燃冰”的可燃成分是甲烷 D.“可燃冰”有可能成为人类未来的重要能源
(4)结合低碳生活的主题,下列说法错误的是。
A.提倡植树造林,严禁乱砍滥伐树木
B.提倡乘坐公共交通方式出行,严禁驾驭私家车出行
C.提倡使用电子邮件、MSN等即时通讯工具,禁用打印机和传真机
D.提倡使用节能技术和节能用具,逐步禁止进口和销售普通照明白炽灯
(5)生活中少买一件不必要的衣服可以节约2.5 kg标准煤(已知标准煤的平均含碳量为72%),则相应减排二氧化碳kg。
请根据下列装置图,回答有关问题: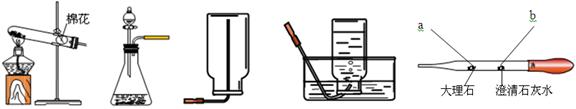
A B CD E
(1)写出实验室在A装置中用高锰酸钾制取氧气的化学方程式:。
(2)实验室收集氧气可用(填编号)装置;在收集过程中,当氧气充满集气瓶后,将导管从瓶口处移开,在桌上。
(3)微型实验有低碳、节约、环保等优点,只要我们善于观察和思考,就能挖掘微型实验的素材和方法。如图E所示,用稍作加工的胶头滴管,吸取几滴稀盐酸,就可以进行二氧化碳的生成与性质微型实验。其中,b处发生反应的化学方程式为。已知H2S是一种剧毒气体,能与氢氧化钠溶液、氧气、氯气、二氧化硫等物质反应。若用此胶头滴管进行H2S实验,避免H2S气体排放到空气中、污染空气的一种方法是。
现有四种物质:①石墨、②干冰、③氮气、④酒精
请选择相应物质的序号填空:
(1)空气中含量最多的气体是;(2)实验室中常用的燃料是;
(3)可用于人工降雨的物质是(4)可用于制铅笔芯的物质是。
右图是元素周期表的一部分。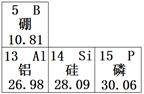
(1)原子序数为15的元素属于(填“金属”或“非金属”)元素。
(2)Al2O3中铝元素的化合价为。
(3)硼元素的原子核外有个电子。