实验室常用溶质质量分数为6%的H2O2溶液(MnO2作催化剂)制取少量氧气。
(1)配制6%的H2O2稀溶液
①计算:市售H2O2溶液溶质质量分数通常为30%。配制100g 6%的H2O2溶液,需要30%的H2O2溶液质量为 g。
②配制:量取所需H2O2溶液和水于烧杯中,用 (填仪器名称)搅拌,充分混合。
(2)制取氧气(可能用到的部分装置如图)
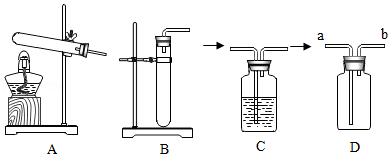
①实验室用H2O2制取氧气的化学方程式为 ,可选择的发生装置为 (填字母)。
②若用C装置干燥氧气,则C中盛放的试剂为 。
③若用D装置收集氧气,则气体应从导管 (填“a”或“b”)端通入。
(3)拓展延伸
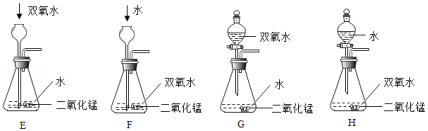
若直接用30%的H2O2溶液制取氧气,反应速率太快。为获得平稳的气流,如图所示发生装置能达到最佳效果的是 (填字母)。
兴趣活动小组设计并完成了如下实验(装置气密性良好,药品足量):
|
操作 |
现象 |
结论 |
装置 |
|
实验一: 同时将Ⅰ中5mL5%的过氧化氢溶液和Ⅱ中 mL15%的过氧化氢溶液注入各盛有0.5g二氧化锰的甲、乙中,关闭弹簧夹。 |
发现烧杯中右侧导管口产生气泡的速率比左侧快。 |
化学反应速率与 有关; 该反应的化学方程式为 。 |
|
|
操作 |
现象 |
现象分析 |
装置 |
|
实验二: 先将稀盐酸注入甲,关闭弹簧夹;再将水注入乙,关闭弹簧夹。 注意:注入液体后,甲、乙导管口均处于液面以下。 |
甲中液体先流入烧杯,乙中液体后流入烧杯,然后观察到烧杯中先无明显现象,后有白色沉淀产生。 |
乙中液体流入烧杯的原因是 ; 甲中流入烧杯的液体溶质的化学式是 。 |
|
如图是实验室制取气体的常用装置.请回答下列问题:

(1)实验室用高锰酸钾制取并收集O 2,选用的装置是 (填字母),为防止试管炸裂,实验中需要注意的事项是 (写出一点),该反应的化学方程式为 ;
(2)用排水法收集O 2用于铁丝在氧气中燃烧的实验,何时停止收集O 2? ;
(3)实验室制取CO 2的化学方程式为 ,用C装置收集CO 2时,导管伸至接近集气瓶底部的原因是 ,验满的方法是 .
利用如图装置进行气体的制取实验,请回答下列问题:

(1)写出标号a仪器的名称: .
(2)用氯酸钾制取氧气的化学方程式 ,选择④装置收集氧气,气体从 (填字母)端进入.若改用排水法收集,实验结束后先撤导气管后熄灭酒精灯,目的是防止 .
(3)实验室用大理石和 (填写药品名称)反应制取二氧化碳.与②相比,③作为发生装置的优点是 ,在装置④中盛放 可用于干燥二氧化碳气体.
如图是初中化学的一些基本实验,请回答相关问题:

(1)A实验中热水的作用是 。(答一点即可)
(2)B实验反应的实质是 。
(3)C实验中澄清的石灰水没有变浑浊,原因是 。(答一点即可)
(4)D实验中两支蜡烛依次熄灭,说明二氧化碳具有的化学性质是 。
某兴趣小组的同学从超市购买一袋食盐,欲检测其是否为加碘食盐(加碘食盐中的碘元素以碘酸钾的形式存在,碘酸钾的化学式为KIO 3).他们査阅资料得知,加碘食盐中的KIO 3在酸性条件下能与KI溶液发生反应,生成碘(I 2),淀粉遇I 2变蓝色.
现提供下列试剂和生活中常见的物质:
①KI溶液②纯碱③米汤④白糖⑤白酒⑥白醋,该小组同学进行实验必须选用的试剂和物质是 .
A.①③④B.①③⑥C.②④⑥D.①④⑤
该小组经过实验确定这袋食盐是加碘食盐,同学们探究的兴趣高涨,他们仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行实验探究.
问题一:食盐是比较稳定的,而说明中强调"防热",是否因为受热会造成碘的损失?
【实验一】探究温度对碘损失率的影响.
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
|
温度 |
30℃水浴 |
50℃水浴 |
80℃水浴 |
100℃水浴 |
煮沸 |
|
碘损失率(%) |
0 |
0.3 |
0.67 |
1 |
5.56 |
分析上表可得出的结论是 .
问题二:炒菜时加醋对碘的损失率是否也有影响?
【实验二】探究酸碱度对碘损失率的影响.
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的 均相同,溶液的酸碱度不同的条件下进行.
(2)实验需要调节溶液的酸碱性,下列物质不能选用的是 (填字母)
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋.