海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
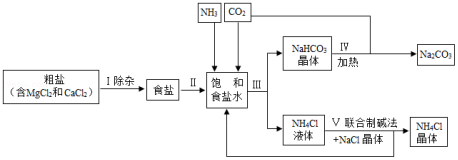
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
阅读下面科普短文
2020年3月8日,面对口罩核心材料熔喷布的需求井喷,国务院国资委指导推动相关中央企业加快生产线建设,为新冠肺炎疫情防控提供保障。
熔喷布主要以聚丙烯[(C3H6)n]为原料,纤维直径可以达到1~5微米,具有独特的毛细结构超细纤维,从而使熔喷布具有很好的过滤性、屏蔽性、绝热性和吸油性,是良好的口罩材料。
聚丙烯是丙烯(C3H6)的聚合物。全球丙烯的工业化生产工艺主要有裂解法、催化裂化法(FCC),甲醇制烯烃(MTO/MTP)、丙烷脱氢(PDH)和烯烃歧化法等,我国和全球丙烯的工业化生产工艺方法及份额分别如图1、图2所示:

中国丙烯产能扩张速度稳定,未来产能增量以PDH为主,因PDH的主要成本来自于原料丙烷,丙烷价格越低廉,项目盈利越可观。因此丙烯作为化工领域中重要的基础原料产品,合理布局及发展烯烃产业结构尤为重要。
依据文章内容,回答下列问题:
(1)口罩的核心材料熔喷布主要以 为原料,它是有机合成材料,而日常生活中用得最多的有机合成材料是塑料、 、合成橡胶。
(2)熔喷布是良好的口罩材料,是因为它具有很好的 、 等优点(任写两点)。
(3)写出丙烯完全燃烧的化学方程式 。
(4)一定条件下,丙烷气体(C3H8)分解可以制得丙烯气体,写出该反应的化学方程式 。
(5)我国生产丙烯份额最多的方法是 ;由图2可知2015﹣2025年,全球各地区采用裂解和FCC生产丙烯份颜均有下降趋势,而 工艺法所产丙烯份额有逐步上升趋势。
水是常用溶剂,某同学进行如图实验。

(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是 。
(2)实验可知,溶质状态可以是 。
(3)实验结束后,用洗涤剂洗净B试管,原理是 。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知:2KMnO4+16HCl(浓)═2KCl+2X+5Cl2↑+8H2O,X的化学式为 。
(5)询问老师得知用2NaOH+Cl2═NaCl+NaClO+H2O可处理Cl2。根据化学方程式计算,处理0.142g Cl2至少需NaOH的质量是多少?
嘌呤是合成DNA的主要物质,广泛存在于细胞核中,嘌呤的化学式为C5H4N4,在人体内会被氧化成尿酸,血液中尿酸含量过高容易引起痛风。
(1)嘌呤的相对分子质量为 。
(2)嘌呤中碳元素和氢元素的质量比为 。
按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管。环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。
(1)纤维素是一种 (选填“有机物”或“无机物”)。
(2)纤维素分子中,氢、氧原子的个数比为 。
(3)计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
|
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。
