支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )

| A. |
通入保护电流使钢管桩表面腐蚀电流接近于零 |
| B. |
通电后外电路电子被强制从高硅铸铁流向钢管桩 |
| C. |
高硅铸铁的作用是作为损耗阳极材料和传递电流 |
| D. |
通入的保护电流应该根据环境条件变化进行调整 |
下列物质一定不是天然高分子的是()
| A.橡胶 | B.蛋白质 | C.聚乙烯 | D.纤维素 |
在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是()
| A.CH4和C2H4 | B.CH4和C2H6 | C.C2H4和C2H6 | D.C3H4和C3H6 |
在理论上可用于设计原电池的化学反应是()
| A.2Al(s)+2NaOH(aq)+2H2O(1) = 2NaAlO2(ag)+3H2(g)△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s)= BaCl2(aq)+2NH3·H2O(aq)+8H2O(l) △H >0 |
| C.CaC2(s)+2H2O(1) = Ca(OH)2(s)+C2H2(g)△H <0 |
| D.HCl(aq)+NaOH(aq) = NaCl(aq) + 3H2O(l)△H <0 |
下图中a、b、c、d、e为周期表前4周期的一部分,下列叙述正确的是()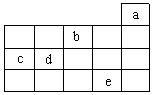
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素形成的单质性质最稳定 |
| C.c、d元素最高价氧化物的水化物酸性:c > d |
| D.e元素在自然界中主要存在于海水中 |
下列说法正确的是()
| A.由H形成1 mol H-H键要吸收热量 |
| B.所有燃烧反应都是放热反应 |
| C.16g O3单质中含有的分子个数为NA |
| D.凡经加热而发生的化学反应都是吸热反应 |