某“自加热食品”发热包的主要成分为生石灰、活性炭、铝粉、铁粉、碳酸钠和氯化钙,其使用说明(如图1所示):

某化学兴趣小组对发热包进行了如下探究。
探究Ⅰ:发热包的发热原理
将发热包中固体倒入烧杯中,加入适量的水,发生剧烈反应,水很快沸腾。反应结束后,烧杯底部有大量固体,继续加水搅拌,过滤、洗涤、干燥,得到固体混合物。
(1)发热包中的某种物质与水反应放出大量的热,该物质的化学式是 。
探究Ⅱ:固体混合物的成分
【查阅资料】单质铝既能与盐酸反应又能与氢氧化钠溶液反应,并产生氢气。
小组同学认为固体混合物的成分可能是:活性炭、铝粉、铁粉、碳酸钙和氢氧化钙。为进一步探究其成分,小组同学设计并进行如下实验:
(2)取少量固体混合物于试管中,加水振荡,静置,滴入几滴酚酞溶液,溶液变为 色,证明该固体混合物中含有氢氧化钙。
(3)另取少量固体混合物于锥形瓶中,逐渐加入稀盐酸至不再产生气泡为止(如图2所示),反应停止后瓶底有黑色固体剩余,溶液呈浅绿色。
①反应停止后,瓶底的黑色固体为 ,判断依据是 。
②若观察到烧杯中澄清石灰水变浑浊,证明该固体混合物中含有 ,对应此现象的化学反应方程式是 。
(4)设计实验方案证明该固体混合物中含有铝粉 。
(包含实验步骤、产生现象和结论。可供选择的试剂:稀盐酸、 溶液、 溶液)。
化学小组的同学探究二氧化碳与氢氧化钠的反应.实验方案如下:
| 实验装置 |
实验步骤及操作 |
实验现象 |
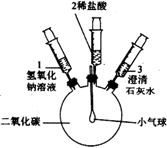 |
①将注射器1中的溶液推入充有CO2的瓶中 |
气球鼓起 |
| ②…… |
无明显现象 |
|
| ③将注射器2中的溶液推入瓶中 |
溶液中有气泡产生,气球变瘪 |
|
| ④向外拉注射器3 |
澄清石灰水变浑浊 |
(1)步骤①中气球鼓起的原因可能是____________________________________________
________________________________________________________________________.
(2)步骤②中的操作是________________________,其目的是________________________.
(3)步骤④中发生反应的化学方程式为________________________________________
________________________________________________________________________.
(4)本实验的结论是________________________________________________________.
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有________性,使纸中的纤维素炭化的缘故;在洗气瓶中盛放浓硫酸,除去氢气或氧气中的水分,是利用其________性.
(2)探究浓硫酸的吸水性.兴趣小组把98%的硫酸10mL和63.3%的硫酸(用10mL 98%的硫酸与10mL水配成)约20mL分别放入两个相同的大表面皿中,称量、观察、记录、分析.根据室温环境下实验的数据绘成的曲线如下图:
①释浓硫酸时,应将________缓缓地注入盛有________的烧杯中并不断搅拌.
②由下图曲线你能得到的实验结论有哪些?(写两点)
________________________________________________________________________;
________________________________________________________________________.
(3)探究浓硫酸能否使铁钝化(钝化指在表面形成氧化膜保护层,使内层金属不再发生变化).
可选用的实验药品有:相同铁片若干、浓硫酸、稀硫酸、硫酸铜溶液等.实验仪器任选.
①兴趣小组已经完成下表实验Ⅰ和Ⅱ,请你帮他们将实验报告补充完整.
| 方案 |
实验 假设 |
实验方案 |
实验现象 与结论 |
| Ⅰ |
能发生钝化 |
取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中 |
无明显变化,假设成立 |
| Ⅱ |
能发生钝化 |
取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中 |
________,假设成立 |
你认为方案Ⅱ与方案I相比,方案Ⅱ的优点是
________________________________________________________________________.
②请你选用提供的药品再设计一个实验,简述实验方案________________________________.
③某同学将一铁片插入盛有98%的浓硫酸的试管中,无明显变化,再给试管加热一段时间后,发现溶液变色并有刺激性气味气体产生,此现象说明:________________________
________________________________________________________________________.
小刚和小丽两位同学用图所示装置进行实验,验证二氧化碳与氢氧化钠、氢氧化钙都能发生反应.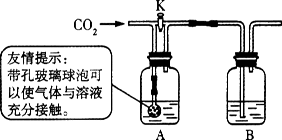
(1)小刚关闭K,通入二氧化碳,A、B中均无明显变化.B中盛放________溶液.
(2)小刚打开K,继续通入二氧化碳.B中反应的化学方程式为________.
此步的实验目的是________.
小丽认为:通常状况下,1体积水约能溶解1体积的二氧化碳,因此上述实验不足以证明二氧化碳和氢氧化钠发生了反应.
(3)小丽用洗涤干净的上述装置重新做实验,分别量取50mL上述溶液放入A、B中,关闭K,通入约500mL二氧化碳,A、B中均无明显变化.此实验可以说明二氧化碳和氢氧化钠发生了反应,其理由是________.
KOH溶液中含有H2O、K+、OH-,能使无色酚酞溶液变成红色.某化学兴趣小组想探究KOH溶液使无色酚酞溶液变成红色的原因.
[提出问题]KOH溶液中的什么成分使无色酚酞溶液变红?
[猜想]猜想1:KOH溶液中的H2O使无色酚酞溶液变红.
猜想2:KOH溶液中的K+使无色酚酞溶液变红.
猜想3:KOH溶液中的________(填化学式)使无色酚酞溶液变红.
[实验探究]
| 实验操作 |
实验现象 |
结论 |
| ①用试管取少量蒸馏水,滴入1~2滴无色酚酞溶液 |
试管内溶液不变色 |
猜想1不成立 |
| ②用试管取少量KCl溶液,滴入1~2滴无色酚酞溶液 |
________ |
猜想2不成立 |
| ③________,滴入1~2滴无色酚酞溶液 |
试管内溶液变红 |
________ |
[讨论反思]有同学认为猜想①不需要实验验证就可以排除,你认为该同学理由是________________.
[拓展]①向Ba(OH)2溶液中滴入几滴无色酚酞溶液,观察到的现象是________________________________;
②KOH固体应________保存.
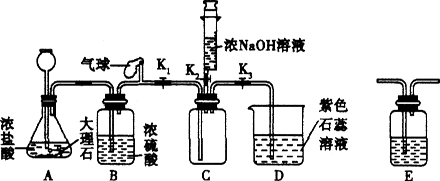
同学们利用如下装置验证CO2能与NaOH反应.(装置气密性良好)
(1)打开K1、K3,关闭K2,当D中出现________的现象时,可确定C中收集满CO2.
(2)C中收集满CO2后,关闭K1,打开K2,将注射器中5mL浓NaOH溶液推入C中,观察到D中液体流入C中,说明CO2与NaOH发生了反应.
①小明发现此装置有明显不足,认为应该在________(填装置字母序号)之间增加洗气瓶E,其作用是________.
②改进装置后,小红认为要想证明CO2与NaOH发生反应,还应利用上述装置补充一个对比实验,实验方案是________.