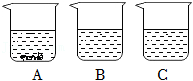
学习《物质的溶解》时小科同学进行了如下实验:往A、B、C三只烧杯中分别装入等质量的水,在相同温度下,向三只烧杯中分别加入50g、25g、5g同种固体物质,充分溶解后,静置,现象如图所示。
回答下列问题:
(1)小科认为,A烧杯中的溶液一定是饱和溶液。他的判断依据是 ;
(2)A、B、C三只烧杯中,溶液的溶质质量分数大小关系是 。
去年,有媒体报道面条可燃,一些市民据此担心面条中加入了不安全的添加剂。
⑴仅从面条可燃就判断加入了添加剂是不科学的,因为面粉含有的主要营养素淀粉本身是可以燃烧的,淀粉的化学式为(C6H10O5)n,完全燃烧的产物是___________、____________(填化学式);燃烧过程中还可闻到像头发烧焦似的刺鼻气味,是由于面粉中另一种营养素燃烧产生的,该营养素是____________。
⑵面粉不仅可以燃烧.一定条件下还会发生爆炸。2010年2月我国某大型面粉厂灌装车间发生面粉爆炸,造成重大人员伤亡。为避免类似事件,生产过程可采取的措施有________________。
| A.密封门窗,隔绝氧气 | B.严禁吸烟,杜绝火源 |
| C.轻拿轻放,减少粉尘扬起 | D.提高淀粉的着火点 |
下图是转化汽车尾气中有害气体的微观示意图。
(1)反应前的图示中含有种分子;
(2)图中所示的化学方程式;
(3)从图中你还能获取的信息是。
我国的酒文化源远流长,民间常有“以酒会客”的习俗,其国酒 “茅台”更是中外闻名。请你回答下列问题:
(1) “茅台”开瓶十里香,这表明分子具有的性质。
(2)“茅台”的主要成分之一是乙醇,其化学式为。
(3)“开车不喝酒,喝酒不开车”。今年国家对“酒驾”给予了更严厉的处罚。交警用“酒精检测仪”很快可以检测出司机的饮酒程度,其化学反应原理是:
C2H5OH+4X+6H2SO4 = 2Cr2(SO4)3 + 2CO2↑+9H2O
化学方程式中X的化学式。
请在H、O、N、Na这四种元素中选择恰当的元素,组成一种符合要求的物质,并将其化学式填写在相应的位置上。
(1)由三种元素组成的酸:。
(2)由三种元素组成的碱:。
(3)由三种元素组成的盐:。
(4)空气污染物中会造成酸雨的氧化物:。
在氦气、硝酸铵、甲烷、活性炭四种物质中,属于最简单有机物的是_①__,可用来填充飞艇的是__②__,可用作化肥的是__③,可用作冰箱除味剂的是__④__(填化学式)。