登山运动员登山时常用氢化钙作为供氢剂,用来提供能源。某兴趣小组同学对放置了一段时间的氢化钙取样进行探究。
【查阅资料】氢化钙( )是一种固态储氢物质,它遇水剧烈反应释放出氢气,反应的化学方程式为 。
【提出问题】该氢化钙样品与水反应是否还能生成氢气?
【实验1】小组同学用适量氢化钙样品和水进行实验。

(1)如图所示是小组同学设计的两个实验装置,为便于控制反应速率,最好选用装置_____(选填“A”或“B”)。
(2)连接好装置后,加入药品前,应进行的操作是_____。
(3)向装置中加入药品并开始实验。锥形瓶中快速产生气泡;将导管插入肥皂水中,吹出肥皂泡,用燃着的木条靠近上升到空中的肥皂泡,肥皂泡被点燃。“肥皂泡被点燃”是因为氢气具有_____性。
【得出结论】该氢化钙样品与水反应还能生成氢气。
【提出新问题】实验1中不再产生气泡后,锥形瓶中有较多白色浑浊物。白色浑浊物是什么?
【分析讨论】氢化钙与水反应生成了氢氧化钙,氢氧化钙微溶于水,白色浑浊物中一定含有氢氧化钙:氢化钙在保存过程中可能变质生成碳酸钙,故白色浑浊物中还可能含有碳酸钙。
【实验2】按图1所示,将白色浑浊物装入锥形瓶中,用注射器注入适量稀盐酸,并利用二氧化碳传感器测得锥形瓶中二氧化碳的体积分数随时间的变化如图2所示。

(4)实验2中锥形瓶内发生反应的化学方程式为_____(写一个即可)。
(5)图2中说明有二氧化碳生成的依据是_____。
【得出结论】白色浑浊物中含有氢氧化钙和碳酸钙,同时说明氢化钙样品有少量变质。
【反思拓展】
(6)保存氢化钙的一条建议是_____。
(7)氢能有很多优点,如_____(写一条即可)。我们共同努力,助力我国早日进入“氢能经济”时代。
如图所示装置(气密性良好),改变滴管和小烧杯中的物质可以完成多个简单实验。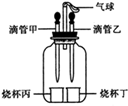
(1)若滴管甲中吸有水,烧杯丙中盛有适量生石灰。将滴管甲中的水滴入烧杯丙中,可观察到气球鼓起,一段时间后装置恢复原状。利用所学化学知识解释气球鼓起的原因是,烧杯丙中发生反应的化学方程式为。
(2)若烧杯丁中盛有适量锌粒,将滴管乙中的液体滴入烧杯丁中,烧杯丁中有气泡生成,气球明显鼓起,则滴管乙中所装液体是,烧杯丁中发生反应的化学方程式为。
(3)若滴管甲中吸有稀硫酸,滴管乙中吸有水,烧杯丙中盛有适量小苏打,烧杯丁中盛有用石蕊溶液染成的紫色干燥纸花。该实验可用于验证使石蕊变色的物质是碳酸而不是二氧化碳。正确的操作顺序是:先,观察;再。
(4)若在丙烧杯中盛有40g溶质质量分数为10%的NaOH溶液,将稀H2SO4通过滴管甲滴入烧杯丙中至恰好完全反应。求:参加反应的NaOH溶液中溶质的质量和反应生成Na2SO4的质量分别为多少克?
珍珠粉以其良好的养颜等功效,获得消费者喜爱。资料显示:珍珠中含碳酸钙80—93%、蛋白质4—14%、水份2—4%、十几种氨基酸、28种微量元素。然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠。以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案。
【探究一】辨别市售珍珠真与假。
将其分别溶于水,充分搅拌、静置,测定上层清液的pH;若pH7(填“>”或“<”或“=”)为假珍珠,理由是。
【探究二】测定珍珠中碳酸钙含量。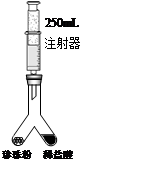
小王用图所示装置测定该珍珠粉中碳酸钙的含量。实验方案如下:
⑴检查装置气密性:按图连接装好置后,将注射器活塞(不考虑活塞的摩擦和自重,下同)从刻度1mL处向上拉至刻度20mL处,(填操作和现象),则气密性良好;
⑵在图异型装置左管内装入1.1g 上述珍珠粉样品,右管内倒入一定量的稀盐酸,注射器(规格为250mL)活塞推到底部,再次连接装置;
⑶设法使左右两管内的药品混合,反应结束后读取注射器读数为220mL;
⑷数据处理:计算得该珍珠粉中碳酸钙的质量分数为。[ρ〔CO2〕=2g/L,结果保留小数点后1位]
【实验思考】
⑴此实验中的反应原理是(用化学方程式表示);
⑵考虑注射器因素,该实验方案对珍珠粉的用量多少是否必须作要求?;
⑶【探究二】中的第⑶步,混合两种药品的方法是;
⑷该实验装置设计上的优点在于(写出1点即可)。
实验室有三瓶不同种类失去标签的盐溶液,均为初中常见的化学物质,分别是碳酸钾溶液、硫酸钠溶液和一种含有钡离子的未知溶液。
【提出问题】如何鉴别出三种溶液?
【实验探究】小松同学:取1号样品溶液少许,加入到一支试管中,向其中滴加适量稀盐酸溶液,没有观察到明显现象,他又继续滴加少量硝酸钡溶液,观察到有白色沉淀产生。他认为1号溶液中的溶质一定不是碳酸钾,一定是硫酸钠。
【反思与评价】请你评价小松同学的实验结论(1);
【实验探究】小北同学:取少量三种样品溶液分别加入到三支试管中,先向各试管中滴加几滴硝酸银溶液,其中2号、3号试管中出现白色沉淀,再加足量稀硝酸,2号试管中出现了(2)现象,说明2号溶液是碳酸钾溶液,3号试管中沉淀无变化。
【表达与交流】同学们经过讨论后认为,最简单的方法是只需要分别滴加一种试剂(3)(填物质化学式)就能将三种溶液鉴别出来。请将三种溶液溶质的化学式分别标在试剂瓶的标签中:(4)。
如右图所示,在250mL干燥的圆底烧瓶中,充满CO2气体,并用带尖嘴导管的单孔塞塞紧(导管另一端的橡胶管事先用夹子夹紧)。实验开始时,先将注射器中的浓氢氧化钠溶液推入到烧瓶中,一段时间后,打开夹子,会观察到的现象有(1),用理化知识解释产生上述现象的原因是(2)。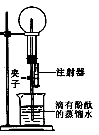
小红同学要通过实验验证二氧化碳能与水反应的性质。请结合右图回答下列问题: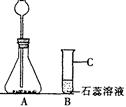
(1)连接A和B并将实验装置图补充完整;
(2)A中发生反应的化学方程式为;
(3)B中观察到的实验现象是;
(4)在一般情况下仪器C的作用是。