中央电视台新闻栏目2006年5月14日报道齐齐哈尔第二制药有限公司生产的假药事件, “齐二药”违反规定,购入工业用“二甘醇”代替医用丙二醇(C3H8O2)作辅料,用于“亮菌甲素注射液”的生产,导致多名患者肾功能衰歇,造成多名患者死亡。二甘醇又称乙二醇醚,分子式为C4H10O3(HO-CH2-CH2-O-CH2-CH2-OH),二甘醇是一种重要的化工原料,可以制取酸、酯、胺等,其主要产品有吗啉及其衍生物1,4-二恶烷( )等被广泛应用于石油化工、橡胶、塑料、制药等行业,用途十分广泛。二甘醇一般的合成路线为:
)等被广泛应用于石油化工、橡胶、塑料、制药等行业,用途十分广泛。二甘醇一般的合成路线为:
 |
 |

|
过程Ⅰ Br2 条件Ⅱ 反应Ⅲ
下列反应属于放热反应的是_______;属于吸热反应的是_______。
| A.锌粒与稀H2SO4反应制取H2 | B.氢气在氧气中燃烧 |
| C.碳酸钙高温分解成氧化钙和二氧化碳 | D.氢氧化钾和硫酸中和 |
E.Ba(OH)2·8H2O与NH4Cl反应 F. C与CO2高温生成CO
G.葡萄糖在人体内 氧化分解 H.钢铁制品生锈的反应
氧化分解 H.钢铁制品生锈的反应
A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比为2∶3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红.请回答下列问题.
(1)Z的离子结构示意图为;化合物BA4的电子式为。
(2)化合物Y2X2 中含有的化学键类型有________(填序号).
中含有的化学键类型有________(填序号).
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是_______(填化学式),其主要原因_____________________。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应生成A2X和Z单质,试写出化学方程式____________________。
氢能是21世纪极具开发前景的新能源之一,
它既是绿色能源,又 可循环利用。请在下图的两个空框中填上循环过程中反应物和生成物的
可循环利用。请在下图的两个空框中填上循环过程中反应物和生成物的 分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转移的角度看,过程Ⅱ主要是能转化为能。
分子式,以完成理想的氢能源循环体系图(循环中接受太阳能的物质在自然界中广泛存在)。从能量转移的角度看,过程Ⅱ主要是能转化为能。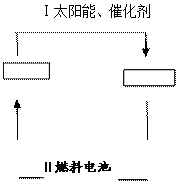
如果用KOH溶液作为电解质溶液,写出该燃料电池的电极反应式
负极:______________________________正极:_________________________________。[来
在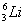 、
、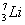 、
、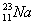 、
、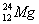 、
、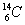 、
、 中:
中:
(1)和互为同位素;
(2)和的质量数相等,但不能互称同位素;
(3)和的中子数相等,但质子数不等,所以不是同一种元素
已知几种难溶电解质的溶度积如下表所示:
| 几种难溶电解质的Ksp(25℃) |
|
| 沉淀溶解平衡 |
Ksp |
AgBr(s) Ag+(aq)+Br-(aq) Ag+(aq)+Br-(aq) |
5,0×10-13mol2·L-2 |
AgI(s) Ag+(aq)+I-(aq) Ag+(aq)+I-(aq) |
8.3×10-17mol2·L-2 |
FeS(s) Fe2+(aq)+S2-(aq) Fe2+(aq)+S2-(aq) |
6.3×10-18mol2·L-2 |
ZnS(s) Zn2+(aq)+S2-(aq) Zn2+(aq)+S2-(aq) |
1.6×10-24mol2·L-2 |
CuS(s) Cu2+(aq)+S2-(aq) Cu2+(aq)+S2-(aq) |
1.3×10-36mol2·L-2 |
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺为:。
(2)向饱和的AgI溶液中加入固体硝酸银,则c(I-)(填“增大”、“减小”或“不变”),若改加AgBr固体,则c(Ag+)(填“增大”、“减小”或“不变”)。
(3)在25℃时,向100mL浓度均为0.1 mol·L-1 FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是(用沉淀物的化学式表示)。
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡: ZnS(s) Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是。
Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是。
| A.加入少量CuS固体 | B.加入少量FeS固体 |
| C.加入少量FeCl2固体 | D.加入少量CuCl2固体 |