下列物质都含杂质(括号内为杂质),试用化学试剂(包括水)除去杂质并进行分离。
(1)乙烷(乙烯、乙炔)
(2)硝基苯(苯)
(3)溴苯(溴)
铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组为测定某含镁3%一5%的铝镁合金(不含其它元素)中镁的质量分数,设计以下实验方案进行探究。填写下列空白。
[实验方案]铝镁合金粉末 测定剩余固体质量
测定剩余固体质量
[实验步骤]
步骤1:称取5.4g铝镁合金粉末样品,投入VmL 2.0mol·L—1NaOH溶液中,充分反应。
步骤2:过滤、洗涤、干燥、称量固体。
[交流与讨论]
(1) 实验中发生反应的化学方程式是;
(2)参与反应的NaOH溶液的体积V≥;
(3)步骤2中,如果经两次过滤滤液仍浑浊,则原因可能是_________(只填一点);
(4)步骤2中,若未洗涤固体,测得镁的质量分数将(填“偏高”或“偏低”)。
[实验拓展] 请你另设计一个实验方案(用上述方案的试剂),测定该铝镁合金中镁的质量分数。
要求:从下图中挑选所需的仪器,画出该方案的实验装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置不用画),并标明所用试剂.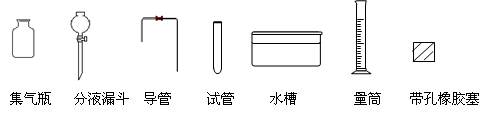

硫酸亚铁铵的化学式为(NH4)2SO4·FeSO4·6H2O,商品名为莫尔盐。可由硫酸亚铁与硫酸铵反应生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:
| 温度/℃ |
10 |
20 |
30 |
40 |
50 |
70 |
| (NH4)2SO4 |
73.0 |
75.4 |
78.0 |
81.0 |
84.5 |
91.9 |
| FeSO4·7H2O |
40.0 |
48.0 |
60.0 |
73.3 |
- |
- |
| (NH4)2SO4•FeSO4•6H2O |
17.2 |
26.4 |
33.0 |
46.0 |
— |
— |
(一)实验室制取少量莫尔盐的流程如下: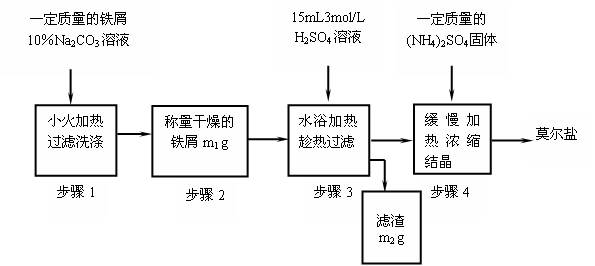
试回答下列问题:
(1)步骤1中加入10%Na2CO3溶液的主要作用是除去铁屑表面的油污,简述其除去油污的原理
(2)将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机
(3)步骤4中析出的晶体不含(NH4)2SO4和FeSO4的原因是,理论上制得的莫尔盐的质量为。
(二)称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的KMnO4酸性溶液进行滴定。
(1)滴定时,将KMnO4酸性溶液装在_______(填“酸式”或“碱式”)滴定管。试写出该滴定过程中的离子方程式:_____;
(2)判断该反应到达滴定终点的现象为;
(3)假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为mol/L
重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X射线透视时服用。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如下: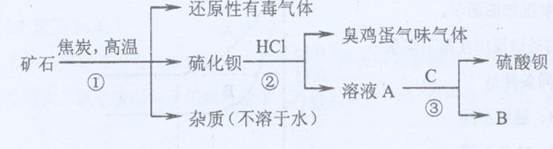 (1)写出步骤①的化学反应方程式,该反应产生的气体具有、等用途。
(1)写出步骤①的化学反应方程式,该反应产生的气体具有、等用途。
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是。在此之前要在溶液中滴入少量Ba(OH)2溶液,其作用是。
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:。
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:。此时若要B物质还能循环使用,则C为(写化学式)。
(5)BaSO4是因为具有、等性质而可用作“钡餐”的。
化学兴趣小组对用铜制取硫酸铜晶体的实验方案作研究。甲组同学将铜粉投入盛有稀硫酸的容器中,不发生反应。他们向容器底部缓缓鼓入氧气,溶液慢慢变蓝色,若在溶液中置一些铂丝,反应速率明显加快。此时,其他组的同学提出方案如下:
(1)甲组实验可用一个化学反应方程式表示为,使反应变快的可能原因是。
(2)在五个方案中,科学性有错的是组方案,经济性最差的是组方案。
(3)可持续发展的原则要求化工生产①能耗尽量低,这应排除使用组方案;②无污染,这应排除组方案。
(4)相对能耗低,污染小的是组方案。该给从反应器中排出的溶液中(含有少量H2SO4以抑制水解)取得产品的实验操作步骤应为、、,对取得产品后残留物质的处理方法是。
Ⅰ.玻璃棒是中学化学实验室中常用的仪器。下列实验过程中,一般不需要用玻璃棒的是
(填写编号)
①用pH试纸测定Na2CO3溶液的pH ②配制一定物质的量浓度的氯化钠溶液③将适量氯化铁饱和溶液滴入沸水中制备氢氧化铁胶体④探究Ba(OH)2 8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
8H20晶体和NH4Cl晶体反应过程中的能量变化⑤用蒸馏法分离两种沸点差距较大的液体⑥过滤分离互不相溶的固体和液体⑦用已知浓度的盐酸滴定待测浓度的NaOH溶液的酸碱中和滴定过程⑧稀释浓H2SO4的过程
Ⅱ.为测定某含有杂质Na2O的Na2O2样品的纯度,某小组同学分别设计了如下方案。
【方案一】准确称量样品mg,与水充分反应后将溶液的体积稀释为VmL,从中取出V1mL溶液,装入锥形瓶,用已知浓度的盐酸进行滴定,以确定溶液的浓度,再计算出样品中Na2O2的含量。
⑴此方案中,酸碱中和滴定时应选用滴定管。
⑵写出此方案中涉及到的反应的离子方程式。
【方案二】准确称量样品mg,将样品与二氧化碳充分反应,通过测定反应产生氧气的体积,计算出样品中Na2O2的含量。
⑶该方案的实验过程中,仪器的连接顺序是(填仪器下方序号),①中的进气口为(填“A”或“B”)
⑷装置⑤的作用是。
⑸你认为方案一、方案二中测定结果比较准确的是。