将12.4克NaOH和NaHCO3组成的固体混合物质于密封容器中,加热到250,度,经充分反应排出气体,冷却后称量剩余固体质量为10.6克,试求原混合物种的NaOH的质量分数。
将Fe2O3、Al2O3两种固体混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答: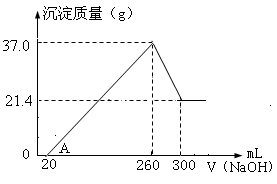
(1)A点坐标(20,0),0到A点的离子反应方程式为
(2)原混合物中Fe2O3的质量是g
(3)所用NaOH溶液物质的量浓度为多少?
解题过程:
(4)稀硫酸物质的量浓度为多少?
解题过程:
24、在标准状况下,4.48L的NH3气体物质的量为mol质量为g,其中含
个氢原子, 将其溶于水配成200mL的溶液,其物质的量浓度为_mol/L。
由Na2CO3·nH2O与NaHCO3组成的混合物28.2 g,放入坩埚中充分加热至质量不变时,将残留固体用足量的盐酸溶解可产生标准状况下的气体3.36 L;若将28.2 g原混合物与盐酸反应,则放出标准状况下气体4.48 L,由此计算。
(1)残留固体质量;
(2)n值;
(3)NaHCO3质量。(写出计算求解的过程)
(12分)化学需氧量(COD)常作为衡量水体中有机物含量多少的指标。某化学课外小组的同学拟采用碱性高锰酸钾溶液测定某海水试样的COD,实验流程如下: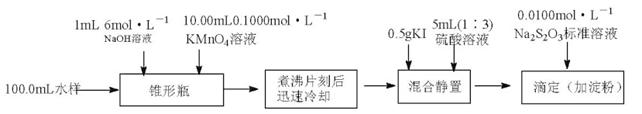
已知:①弱碱性条件下MnO4-被还原性物质还原为MnO2
②10I-+2MnO4-+16H+=5I2+2Mn2++8H2O
③2S2O32-+I2=2I-+S4O62-
(1)测定海水试样的COD,采用碱性高锰酸钾溶液而不采用酸性高锰酸钾溶液,其可能原因是。
(2)氧化后的水样煮沸后,需冷却并在暗处再加入KI和硫酸,需在暗处的原因是。用Na2S2O3,标准溶液滴定,终点时溶液颜色的变化是。
(3)滴定到终点时消耗Na2S2O3标准溶液10.00mL。根据以上实验数据计算海水试样的COD(用每升水样相当于消耗多少毫克O2表示,单位:mg•L-1)(写出计算过程)。
矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示。
(1)CaxMgySi8O22(OH)m改写成氧化物的形式为,化学式中x、y、m的代数关系式为。
(2)对矿物样品粉末灼烧至恒重,则减少的质量与灼烧后固体中Si元素的质量比为(用m表示)。
(3)为确定CaxMgySi8O22(OH)m的组成,进行如下实验:
①准确称取8.10g样品粉末,加入足量稀盐酸充分溶解,过滤,将沉淀灼烧得固体4.80g。
②另准确称取16.20克样品粉末在空气中灼烧,样品减少的质量随灼烧时间的变化如图所示。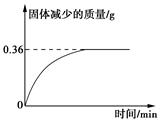
根据以上实验数据计算样品的化学式(写出计算过程)。