在常温常压下的以下物质①10mL水②100mL氯气③220mL氖④120mL二氧化碳,这四种物质中所含原子数由多到少的顺序是
| A.①②③④ | B.①④③② |
| C.③④②① | D.④③②① |
已知:2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是
| A.H2(g)的燃烧热为571.6 kJ·mol-1 |
B.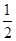 H2SO4(aq)+ H2SO4(aq)+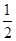 Ba(OH)2(aq)=== Ba(OH)2(aq)===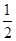 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 |
| C.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 |
| D.3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1 |
甲醇燃料电池(DMFC)可用于汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质溶液是稀硫酸。电池工作时,甲醇被氧化为二氧化碳和水。下列叙述中不正确的是
A.负极的反应式为CH3OH+H2O-6e-===CO2↑+6H+
B.氧气在电极上的反应是O2+4H++4e-===2H2O
C.电池工作时,H+由正极移向负极
D.电池工作时,电子从通入甲醇的一极流出,经外电路流入通入氧气的一极
某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)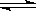 Z(g)+W(s) △H>0,下列叙述正确的是
Z(g)+W(s) △H>0,下列叙述正确的是
| A.加入少量W,逆反应速率增大 |
| B.当容器中气体压强不变时,反应达到平衡 |
| C.升高温度,平衡逆向移动 |
| D.平衡后加入X,上述反应的△H增大 |
今有A、B两种原子,A原子的M层比B原子的M层少3个电子,B原子的L层电子数恰为A原子L层电子数的2倍,A和B分别是
A.Si和Na B.B和H C.Cl和CD.C和Al
在容积不变的密闭容器中发生反应2NO2 (g)  2NO(g)+O2(g),能说明该反应已达化学平衡状态的是
2NO(g)+O2(g),能说明该反应已达化学平衡状态的是
①生成n mol O2的同时生成2n mol NO2 ②生成n mol O2的同时生成2n mol NO
③v(NO2)∶v(NO)∶v(O2)=2∶2∶1 ④混合气体的颜色不再改变
⑤混合气体的密度不再改变 ⑥混合气体的平均相对分子质量不再改变
| A.①④⑥ | B.②③⑤ | C.①③④ | D.④⑤⑥ |