在新型有机高分子材料中,有一种感光高分子材料,也称为光敏高分子,是一种在彩电光屏及大规模集成电路的制造中使用的功能高分子材料,其结构简式为:
已知它是由两种化合物经酯化后聚合而成的,这两种化合物的结构简式为:__________________________。
锂-磷酸氧铜电池正极的活性物质是Cu4O(PO4)2, 可通过下列反应制备: 2Na3PO4+4CuSO4+2NH3·H2O=Cu4O(PO4)2↓+3Na2SO4+(NH4)2SO4+H2O。请回答下列问题。
(1)上述方程式中涉及到的N、 O元素电负性由小到大的顺序是。
(2)基态S的价电子排布式为。与Cu同周期且最外层电子数相等的元素还有(填元素符号)。
(3)PO43-的空间构型是, 其中P原子的杂化方式为。
(4)在硫酸铜溶液中加入过量的KSCN溶液, 生成配合物[Cu(CN)4]2-则1molCN-中含有的π键的数目为。
(5)铜晶体为面心立方最密集堆积, 铜的原子半径为127.8pm, 列式计算晶体铜的密度g/cm3。
(6)下表列出了含氧酸酸性强弱与非羟基氧原子数的关系。
由此可得出的判断含氧酸强弱的一条经验规律是。亚磷酸 (H3PO3) 也是中强酸,它的结构式为 。亚磷酸与过量的氢氧化钠溶液反应的化学方程式为。
下表为元素周期表的一部分, 请参照元素①~⑧在表中的位置, 用化学用语回答下列问题:
(1)画出元素⑦的原子结构示意图_________________________。
(2)②、 ③、 ⑦的最高价含氧酸的酸性由强到弱的顺序是____________ (填化学式)
(3)①、 ④、 ⑤、 ⑨中的某些 ··元素可形成既含离子键又含共价键的化合物, 写出其中一种化合物的化学式: ___________。
(4)写出元素③的气态氢化物与其最高价含氧酸的离子方程式___________________写出元素②的单质与元素⑧最高价含氧酸浓溶液的反应化学反应方程式_______________
(5)由表中元素形成的常见物质X、 Y、 Z、 M、 N可发生以下反应:
X溶液与Y溶液反应的离子方程式为_____________________________。
碳和氮的化合物与人类生产、 生活密切相关。
(1)在一恒温、恒容密闭容器中发生反应:
利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。下列说法正确的是(填字母编号)。
| A.增加Ni的量可提高CO的转化率, Ni的转化率降低 |
| B.缩小容器容积, 平衡右移,ΔH减小 |
| C.反应达到平衡后, 充入CO再次达到平衡时, CO的体积分数降低 |
| D.当4v正[Ni(CO) 4]= v正(CO) 时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态 |
(2)CO与镍反应会造成含镍催化剂的中毒。为防止镍催化剂中毒, 工业上常用SO2将CO氧化, 二氧化硫转化为单质硫。
(3)对于反应: ,向某容器中充入10mol的NO和10mol的O2,在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图)。
,向某容器中充入10mol的NO和10mol的O2,在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图)。
①比较P1、P2的大小关系: ________________。
②700℃时,在压强为P2时, 假设容器为1L,则在该条件平衡常数的数值为_____ (最简分数形式)
(4)NO2、 O2和熔融NaNO3可制作燃料电池, 其原理如图所示。该电池在使用过程中石墨Ⅰ电极上生成氧化物Y, 其电极反应式为。若该燃料电池使用一段时间后, 共收集到20mol Y, 则理论上需要消耗标准状况下氧气的体积为L。
【化学——选修3:物质结构与性质】(15分)稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17 种元素。稀土有“工业维生素”的美称,如今已成为极其重要的战略资源。
(1)钪(Sc)为21号元素,其基态原子M能层电子数为。镝(Dy)的基态原子电子排布式为[Xe]4f106s2,一个基态镝原子所含的未成对电子数为。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是。
几种稀土元素的电离能(单位:kJ·mol-1)
| 元素 |
I1 |
I2 |
I3 |
I1+I2+I3 |
I4 |
| Sc(钪) |
633 |
1235 |
2389 |
4257 |
7019 |
| Y(钇) |
616 |
1181 |
1980 |
3777 |
5963 |
| La(镧) |
538 |
1067 |
1850 |
3455 |
4819 |
| Ce(铈) |
527 |
1047 |
1949 |
3523 |
3547 |
(3)离子化合物 Na3[Sc(OH)6]中,存在的作用力除离子键外还有。
(4)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2。
ICH2CH2I中碳原子杂化轨道类型为,1 mol CH2=CH2中含有的σ键数目为。常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是。
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。则PrO2(二氧化镨)的晶胞中有个氧原子。
(6)Ce(铈)单质为面心立方晶体,其胞参数为a=516pm。晶胞中Ce(铈)原子的配位数为,列式表示Ce(铈)单质的密度:g·cm-3(不必计算出结果)。
(12分)甲醇可作为燃料电池的原料。通过下列反应可以制备甲醇:CO ( g )+2H2 ( g )  CH3OH ( g )
CH3OH ( g )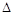 H=-90.8 kJ·mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO 的 平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态B 时,容器的体积为4 L。
H=-90.8 kJ·mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO 的 平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态B 时,容器的体积为4 L。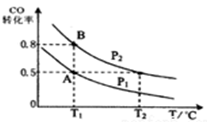
(1)该反应的化学平衡常数表达式为。
(2)如反应开始时仍充入10 mol CO 和20 mol H2,则在平衡状态A时,容器的体积V(A)=L。
(3)关于反应CO(g)+2H2(g) CH3OH(g)建立化学平衡状态时的标志是(填字母)。
CH3OH(g)建立化学平衡状态时的标志是(填字母)。
A.CO的含量保持不变
B.容器中CH3OH浓度与CO浓度相等
C.2V正(CH3OH)=V正(H2)
D.容器中混合气体的平均相对分子质量保持不变
(4)已知CO2(g)+H2(g) CO(g)+H2O(g) H=+41.3 kJ·mol-1,试写出由CO2和H2制取甲醇的热化学方程式。
CO(g)+H2O(g) H=+41.3 kJ·mol-1,试写出由CO2和H2制取甲醇的热化学方程式。
(5)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+氧化成Co3+,然后以Co3+做氧化剂把水中的甲醇氧化成CO2而净化。
实验室用下图装置模拟上述过程: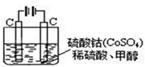
①写出阳极的电极反应式_______________。
②写出除去甲醇的离子方程式__________________。