下图的每一方格中表示有关的一种反应物或生成物,其中A、C、D、E为无色气体,F为红棕色气体。
试完成下列问题:
(1)M可以是____________,E是_____________,F是____________。
(2)反应①的化学方程式是________________________________。反应②的离子方程式是________________________。
(3)F与水的反应中氧化剂与还原剂的物质的量之比为____________。
(4)实验室检验C气体收集满了的方法是_______________________________,实验室检验A气体收集满了的方法是_________________________。
用化学式回答原子序数11~18号元素的有关问题。
(1)除稀有气体外,原子半径最大的是 。
(2)最高价氧化物对应的水化物中碱性最强的是 。
(3)最高价氧化物对应的水化物中呈两性的是 。
(4)最高价氧化物对应的水化物中酸性最强的是 。
(5)形成的气态氢化物中最稳定的是 。
设X、Y、Z代表3种元素。已知:
①X+和Y-两种离子具有相同的电子层结构
②Z元素原子核内质子数比Y元素原子核内质子数少9个
③Y和Z两元素可以形成4核42个电子的负一价阴离子
据此,请填空:
(1)Y元素是_________,Z元素是_________。
(2)由X、Y、Z三元素所形成的含68个电子的盐类化合物的分子式(即化学式)是___________。
紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸和B醇生成的一种酯。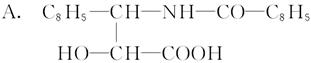
B.R—OH(R是一个含C、H、O的基团)
(1)A可在无机酸的催化下水解,其反应方程式是:__________________________________。
(2)A水解所得的氨基酸不是天然蛋白质的水解产物,因为____________________________。
(3)写出R—OH的分子式_________________________________________________________。
(6分)分类是按照事物的性质划分类别的常用方法。表1是对下列食物的一种分类,请你再找出一种分类方法,完成表2。
①牛奶 ②大米 ③面粉 ④芒果 ⑤胡萝卜 ⑥菠萝 ⑦瘦猪肉 ⑧酸奶 ⑨苹果 ⑩鸡肉
表1食物分类(一)
| 类别 |
食物编号 |
| 乳品类 |
①⑧ |
| 粮食类 |
②③ |
| 蔬菜类 |
⑤ |
| 水果类 |
④⑥⑨ |
| 肉类 |
⑦⑧ |
表2食物分类(二)
| 类别 |
食物编号 |
(4分)青藏地区烧水的水壶,内壁往往结有一厚层水垢。经分析,其主要的成分是CaCO3、MgCO3和Mg(OH)2。由此推测该地区天然水中可能含有的物质是__________。