常温下,有一无色混合气体,可能由Cl2、HCl、NO、O2、CO2、N2、H2、NH3中的两种或多种组成,取此混合气体200 mL进行实验如下:
(1)将此气体通过浓硫酸,体积减少40 mL;
(2)剩余气体通过足量过氧化钠固体,体积又减少40 mL;
(3)剩余气体仍为无色,引燃后冷却至常温,体积又减少105 mL;
(4)最后剩余气体为15 mL,经分析知道其中氧气占1/3。则原混合气体中一定不含________;一定含________,其体积分别是_________。
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色粘稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
| 实验步骤 |
解释或实验结论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍。 |
试通过计算填空: (1)A的相对分子质量为:。 |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重5.4g和13.2g。 |
(2)A的分子式为:。 |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况)。 |
(3)用结构简式表示A中含有的官能团: 。 |
(4)A的核磁共振氢谱如下图: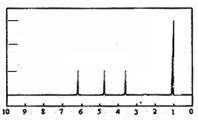 |
(4)A中含有种氢原子。 |
| (5)综上所述,A的结构简式为:。 |
化学式为C8H10O的化合物A具有如下性质:
⑤脱水反应的产物,经聚合反应可制得一种塑料制品(它是目前造成“白色污染”的主要污染源之一)
试回答下列问题:
(1)根据上述信息,对该化 合物的结构可作出的判断是__________(填编号);
合物的结构可作出的判断是__________(填编号);
| A.苯环上直接连有羟基 | B.苯环侧链末端有甲基 |
| C.肯定有醇羟基 | D.肯定是芳香烃 |
(2)化合物A的结构简式为:_______________________;
(3)A和金属钠反应的化学方程式是:__________________________________________________。
(8分)有机物A与乙酸无论以何种比例混合,只要总质量一定,完全燃烧后产生的水的质量也一定,回答:
⑴满足题干条件的A应与乙酸具有相同的___________________。
(2) 若A与乙酸相对分子质量相等,且既能发生银镜反应又能发生酯化反应,则A的结构简式为_____________。
(3)若A由四种元素形成的两种官能团组成,相对分子质量与乙酸相等,且分子中氢原子都不与碳原子相连,则A的结构简式为_____________。
(4)若A分子中氧元素质量分数为13.33%,其余为C、H且其原子个数比为1:1,,且A的相对分子质量小于200,则A的分子式为___________。
下表中括号内物质为所含的少量杂质,请选用适当的试剂和分离装置将杂质除去,并将所选的试剂及装置的编号填入表中:
试剂:①水②氢氧化钠③溴水分离装置:A.分液装置 B.蒸馏装置 C.洗气装置
| 需加入的试剂 |
分离装置 |
|
| 苯(乙醇) |
||
| 乙烷(乙烯) |
||
| 乙醇(乙酸) |
(6分)在一定温度下将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白:
2C(g)+2D(g),2分钟末反应达到平衡状态,生成了0.8 mol D,请填写下面空白:
(1)用B表示的平均反应速率为____________, A的转化率为____________。
(2)如果缩小容器容积(温度不变),则平衡体系中混合气体的密 度____________,混合气体平均相对分子质量____________(填“增大”、“减少”或“不变”)。
度____________,混合气体平均相对分子质量____________(填“增大”、“减少”或“不变”)。
(3)若开始时只加C和D各4/3 mol,要使平衡时各物质的物质的量原平衡相等,则还应加入____________ mol B物质。
(4)若向原平衡体系再投入1 mol A和1 mol B,平衡_______(填“右移、左移或不移”)。