你注意到汽车加油站内的标牌了吗?某些省市加油站提供的汽油标号由90号、93号换成了E90、E93,后者是在汽油中加入了10%的燃料乙醇而制得的乙醇汽油。
燃料乙醇的生产过程可由下图表示:

(1)粉碎玉米的目的是:
(2)生产过程中为了检验淀粉水解是否完全,可使用试剂是
(3)步骤a的操作是
(4)发酵产生的CO2纯度可达到99%,能回收利用,请举出它的两项用途:
(5)以玉米等淀粉原料生产乙醇的化学反应可用下式表示:
根据上述反应式,可以算出100kg淀粉理论上可生产无水乙醇
到目前为止,我国已有上百个地市使用乙醇汽油。
(1)为了便于区分燃料乙醇和食用乙醇,常在燃料乙醇中添加少量煤油,这里利用了煤油的物理性质是:
(2)含10%乙醇的汽油在储存和运输过程中应特别注意防水,如果混入了水,汽油中会出现的现象是
右图是燃料乙醇的生产和消费过程示意图。虽然燃料乙醇的使用缓解了汽车能源的紧张状况,但仍存在一些问题。由此可知,燃料乙醇
除了燃料乙醇,二甲醚(CH3OCH3)和甲醇(CH3OH)也可作为汽车燃料,其中与乙醇互为同分异构体的是
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题。
(1)五种盐中,一定没有的阳离子是 ;所含阴离子相同的两种盐的化学式是 。
(2)D的化学式为 ,D溶液显碱性的原因是(用离子方程式表示) 。
(3)A和C的溶液反应的离子方程式是 ;E和氨水反应的离子方程式是 。
(4)若要检验B中所含的阳离子,正确的实验方法是 。
如图所示,两个连通容器用活塞分开,左右两室(体积相同)各充入一定量NO和O2,且恰好使两容器内气体密度相同。打开活塞,使NO与O2充分反应。(不考虑NO2与N2O4的转化)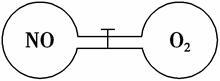
(1)开始时左右两室分子数 (填“相同”或“不相同”)。
(2)反应前后NO室压强 (填“增大”或“减小”) 。
(3)最终容器内密度与原来 (填“相同”或“不相同”)。
(4)最终容器内 (填“有”或“无”)O2存在。
实验是化学学科的基础,也是化学探究的重要方法。
(1)下列有关实验的描述合理的是 (填选项序号)
| A.用玻璃棒蘸取氯水,点在pH试纸的中部测定其pH; |
| B.向冰醋酸中加水,溶液导电性最强时pH最小; |
| C.处理化学实验中产生的废液时,用大量水稀释后冲入下水道; |
| D.为了获得感性认识,可触摸或品尝少量化学药品; |
E.实验室制备乙酸乙酯时,可用盛有饱和NaCl溶液的试管收集产品;
F.酸碱中和滴定时,若用待测液润洗锥形瓶,会导致实验结果偏大。
(2)“铝热反应”在工业生产中具有重要的用途。实验室里用铝粉和氧化铁组成“铝热剂”,引发反应的实验操作是: ;选择恰当的试剂除去产物中混有的少量铝,请写出离子方程式: 。
(12)【有机化学基础】琥珀酸二乙酯是良好的增塑剂和特种润滑剂,也是重要的有机合成的中间体。分析下图中物质间的转化关系,回答问题。
已知:RCN RCOOH
RCOOH
(1)B与D的结构简式分别为 、 。
(2)C的同分异构体中,与C具有相同官能团的是 (写结构简式)。
(3)由C制备琥珀酸二乙酯的化学方程式为: 。
(4)上图转化关系中涉及的基本反应类型有 。
(5)若E为高分子化合物,则由C与D制备E的化学方程式为 。
(6)若E为八元环状化合物,其分子式为 。
(12)【物质结构与性质】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、C、D可形成常见的气态单质,A、E最外层电子数与其电子层数相等。B、F同主族,B元素基态原子核外电子平均分布在3个不同的能级上。C元素原子的最高能级上有3个未成对电子。F的一种单质与FD2晶体类型相同。
(1)A分别与B、F形成的最简单化合物相比较,影响沸点高低的主要作用力是 。
(2)写出D的基态原子的核外电子排布式:___________________。
(3)B、C、D的第一电离能由小到大的顺序为: 。
(4)BD2在高温高压下所形成的晶胞如图所示,该晶体中B原子的杂化方式为__________。
(5)由上述5种元素中的1种或几种形成的,与C的单质互为等电子体的物质是 (填化学式)。
(6)在E的化合物E2Cl6中存在的化学键有 。
a.共价键
b.非极性键
c.配位健
d.σ键
e.π键