五种短周期元素的性质或原子结构信息如下表:
| 元素 |
元素性质或原子结构信息 |
| Q |
原子核外有6种不同运动状态的电子 |
| R |
最外层电子数是次外层电子数的3倍 |
| X |
气态氢化物的水溶液呈弱碱性 |
| Y |
第三周期元素的简单离子中离子半径最小 |
| Z |
单质为银白色固体,在空气中燃烧发出黄色火焰 |
请根据表中信息回答下列问题:
(1)Q原子的电子排布式为___________________________,其同位素有 。
(2)R与Z组成的化合物的化学式是 。
(3)X气态氢化物分子的空间构型为 。X的最高价氧化物对应的水化物其浓溶液与同类物质相比在化学性质上表现的特殊性有 。
(4)Y单质与V2O5反应的化学方程式为 。
(5)在1.01×105Pa、298K时,1.4gQR气体在1.6gR2气体中完全燃烧,生成QR2气体时放出14.15kJ热量,表示QR燃烧的热化学方程式为 。
一定温度下在体积为5 L的密闭容器中发生可逆反应。
(Ⅰ)若某可逆反应的化学平衡常数表达式为:
(1)写出该反应的化学方程式:;
(2)能判断该反应一定达到化学平衡状态的依据是(填选项编号)。
| A.容器中气体的平均相对分子质量不随时间而变化 | B.υ正(H2O)=υ逆(H2) |
| C.容器中气体的密度不随时间而变化 | D.容器中总的物质的量不随时间而变化 |
E. 消耗n mol H2的同时消耗n mol CO
(Ⅱ)某高温下,若该5 L密闭容器中加入的是2molFe(s)与1.00mol H2O(g),t1秒时,H2的物质的量为0.20 mol,到第t2秒时恰好达到平衡,此时H2的物质的量为0.50mol 。
(1) t1~t2这段时间内的化学反应速率v(H2)=。
(2)计算该可逆反应t2达到平衡时的K值。(要求写出计算过程)
(3)该反应的逆反应速率随时间变化的关系如右图。t1时改变了某种条件,改变的条件可能是、。(填写2项)
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。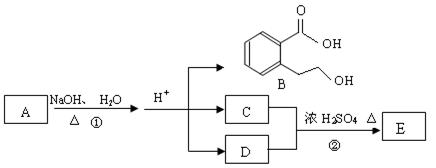
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为; C分子中的官能团名称是 ______________;化合物B不能发生的反应是(填字母序号):
a.加成反应 b.取代反应 c.消去反应 d.酯化反应 e.水解反应 f. 置换反应
(2)反应②的化学方程式是__________________。
(3)反应②实验中加热的目的是:
Ⅰ。;
Ⅱ。。
(4)A的结构简式是 __________________。
(5)同时符合下列三个条件的B的同分异构体的数目有四个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3溶液发生显色反应。写出其中任意一个同分异构体的结构简式。
某芳香烃A有如下转化关系: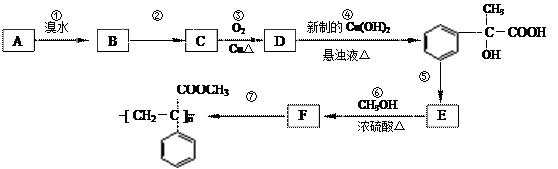
按要求填空:
⑴写出反应②和⑤的反应条件:②;⑤
⑵属于取代反应的有____________ ____________________(填序号)
____________________(填序号)
⑶写出A和F结构简式:A;F
⑷写出反应③对应的化学方程式:,此反应的类型是反应
(5)15g D与足量的银氨溶液反应最多可以生成银mol
(9分)在某有机物A的结构简式如图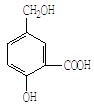
(1)A与NaOH溶液反应的化学方程式是
(2)A与NaHCO3溶液反应的化学方程 式是
式是
(3) A在一定条件下 跟Na反应的化学方程式是
跟Na反应的化学方程式是
I.按要求填空:
(1)羟基的电子式是
(2)羧基的结构式是
(3)(CH3)2C=CHCH2CH3的名称为
II.今有化合物:
(1)请写出丙中含氧官能团的名称:
(2)请判别上述哪些化合物互为同分异构体:
(3)请按酸性由强至弱排列甲、乙、丙的顺序: