离子键的强弱主要决定于离子半径和离子的电荷值。一般规律是:离子半径越小,电荷值越大,则离子键越强。试分析:①K2O ②CaO ③MgO 的离子键由强到弱的顺序是
铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42-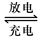 2PbSO4+2H2O
2PbSO4+2H2O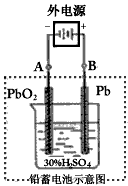
回答下列问题(不考虑氢、氧的氧化还原)
(1)放电时:正极的电极反应式是 ;电解液中H2SO4的浓度将变______,当外电路通过1mol电子时,理论上负极板的质量增加 g。
(2)在完全放电耗尽PbO2和Pb时,若按下图连接,电解一段时间后,则在A电极上生成__________,B电极上生成________,此时铅蓄电池的正负极的极性将____________。
下列物质之间有如下反应关系: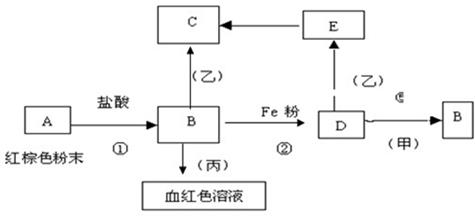
已知由E转化成C的现象是:灰白色沉淀迅速变为灰绿色,最后变为红褐色。
回答:
(1)写出下列物质的化学式:
A B D
甲 乙 丙
(2)写出E→C反应的化学方程式: 。
(10分)下列六个图中,横坐标为某溶液中加入某物质的物质的量,纵坐标为生成沉淀的物质的量,请把下表中各反应的相应图像的序号填入表中。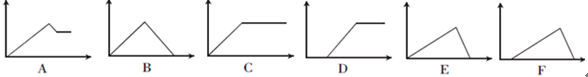
| 溶液 |
加入的物质 |
答案序号 |
| ①饱和石灰水 |
通过量CO2 |
|
| ②AlCl3溶液 |
通过量NH3 |
|
| ③MgCl2、AlCl3混合溶液 |
逐滴加NaOH溶液至过量 |
|
| ④AlCl3溶液 |
逐滴加NaOH溶液至过量 |
|
| ⑤含少量HCl的AlCl3溶液 |
逐滴加NaOH溶液至过量 |
某同学欲在实验室中对Fe3+与I-的反应进行探究,实现Fe2+与Fe3+的相互转化。
(1)该同学最初的实验操作和现象如下:
| 编号 |
操作 |
现象 |
| I |
先向2 mL 0.1 mol/L FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 |
|
| II |
先向2 mL 0.1 mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol/L KI溶液 |
①实验II的预期现象为 。
②FeCl2溶液与新制氯水反应的离子方程式为 。
(2)该同学在进行实验I时,加入的氯水过多,导致出现的红色又褪去,则可能的原因是 。
丙烯是重要的化工原料,一定条件下可发生下列转化:

回答下列问题:
(1)以下化合物中含有羧基的是 。
A.化合物BB.化合物CC.化合物DD.化合物E
(2)上述反应中未涉及的反应类型是 。
A.取代反应B.加成反应C.还原反应D.加聚反应
(3)写出含碳数最少且与D互为同系物的有机物的结构简式___________;写出D与足量乙醇发生反应的化学方程式 。