已知X、Y、Z、W四种元素是元素周期表中三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。试推断:
(1)X、Y、Z、W四种元素的符号:X 、Y 、Z 、W 。元素Z在周期表中的位置是______________________。
(2)由以上元素中的两种元素组成的化合物,溶于水后水溶液显碱性,该化合物的电子式分别为 、 (任写2种)。
(3)由X、Y、Z所形成的共价化合物(Y呈最高价)是 ,离子化合物是 。(均写化学式)
(4)由X和Y两种元素组成的18电子的分子为__________(写分子式),该分子中所有原子都已达到类似于稀有气体原子的稳定结构,则其结构式为__________。
某小组同学要配制100 mL 0.100 mol·L-1 Na2CO3溶液。下图是一些关键步骤和操作。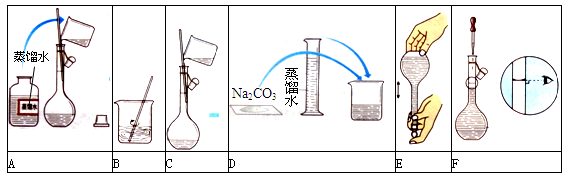
(1)配制过程的先后顺序为(用字母A~F填写)。
(2)配制过程所需的玻璃仪器有烧杯、玻璃棒、量筒、。
(3)若用Na2CO3·10H2O晶体来配制溶液,但晶体已经部分失去结晶水,则所配得溶液的浓度会(填“偏高”、“偏低”、“不变”)。
(4)步骤A通常称为洗涤,如果没有步骤A,则配得溶液的浓度将(填“偏高”、“偏低”、“不变”);步骤F称为,如果俯视刻度线,配得溶液的浓度将(填“偏高”、“偏低”、“不变”)。
(5)在步骤B之后,需才进行下一步操作。
某无色待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入NaOH溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
(1)待测液中一定含有的离子是,一定不含有的离子是。
(2)步骤III中产生气体的离子方程式为。
(8分)
(1)0.5 mol SO2共约含有个原子,它与g SO3所含硫原子数相等。
(2)质量相同的 ①HCl、②NH3、③CO2、④O2四种气体中,含有分子数目最少的是(填序号)。
(3)有100mL 0.2 mol/L 的NaOH溶液,将此溶液稀释到200 mL,则溶液中Na+的物质的量是。
按要求写出下列反应的化学方程式:
(1)过氧化钠与水反应:。
(2)氢氧化铝与氢氧化钠溶液反应:。
(3)浓盐酸与MnO2加热反应制Cl2:。
(4)用小苏打治疗胃酸过多:。
已知NaOH与NaHCO3发生反应的方程式为:
Ⅰ.实验室用氢氧化钠固体配制 的NaOH溶液,回答下列问题:
的NaOH溶液,回答下列问题:
(1)下列操作的顺序是(每项限选一次)_____________。
| A.称量 |
| B.溶解 |
| C.洗涤 |
| D.定容 |
E.转移
F.摇匀
G.冷却
(2)若容量瓶中有少量蒸馏水,所配溶液的浓度将_____________;(填“偏大”、“偏小”或“无影响”)
(3)在定容操作时,俯视容量瓶刻度线,则所配溶液的浓度将_____________(填“偏大”、“偏小”或“无影响”)。
Ⅱ.在 溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
(1)请填写下表空白。
| 编号 |
① |
② |
③ |
④ |
| X的化学式 |
NaOH |
Na2O2 |
||
| 加入X的质量(g) |
9.2 |
15.6 |
(2)反应后,溶液中的Na+的物质的量均为_____________mol。
(3)在①~④中,所得Na2CO3溶质的质量分数相等的是_____________(填编号)。