(15分)
阅读分析材料,据此完成下列要求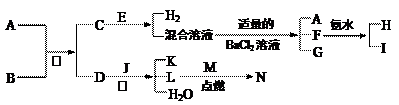 A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
A到N为中学化学常见物质或该物质的水溶液,且它们之间存在如下转化关系
其中,A是生活的必需品,其焰色反应呈黄色;B为二元强酸;D为氢化物;E在地壳中的含量居第三位,其单质大量用于制造导线和合金;J是普通干电池的重要成分;C为酸式盐;F的水溶液与少量的过氧化钠反应也可得到I;G是一种不溶于稀硝酸的白色沉淀;M在L气体中燃烧产生棕黄色烟。
⑴A的晶体类型为 ,C的化学式为 。
⑵M的化学式为 ;若N的水溶液呈蓝绿色,则M与B反应的化学方程
式为: 。
⑶D的浓溶液与J反应的离子方程式为: 。F的水溶液与过量的过氧化钠反应的离子方程式为: 。
⑷H溶液中各离子浓度由小到大的顺序为 。
工业上电解饱和食盐水能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1) 右图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是;NaOH溶液的出口为______(填字母);精制饱和食盐水的进口为_____(填字母);干燥塔中使用的液体干燥剂是____(每空2分)。
(2) 原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加人的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是(2分)(填序号)。
(3) 多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为(2分)。 也可转化为
也可转化为 而循环使用。一定条件下,在200C恒容密闭容器中发生反应:
而循环使用。一定条件下,在200C恒容密闭容器中发生反应: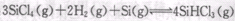 ,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
,达平衡后,H2与SiHCL3物质的量浓度分别为0. 140mol/L和0. 020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的物质的量为_______ (2分)mol。
(4)已知1 g阴极产生的气体在阳极产生的气体中完全燃烧时放出92. 3 kj的热量,则该反应的热化学方程式为: (2分)。
A、B、C、D、E、F均为短周期元素,且原子序数依次增大,A是原子半径最小的元素,B的最髙价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4 : 1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成离子个数比为
2 : 1的离子化合物丙。
(1) D的原子结构示意图为(1分),丙的电子式为,E在周期表中的位置为(2分)。
(2) 下列说法正确的有(2分)。
①化合物乙为正四面体形分子,是由极性键构成的非极性分子
②C、D、E、F原子半径由大到小的顺序为C>D>E>F
③B、E形成的氢化物中,B的氢化物稳定性更强,是因为该分子中存在氢键
④化合物甲和化合物丙都含有离子键和共价键
(3) 已知通常状况下1gF在空气中完全燃烧放出a kj的热量,请写出表示F燃烧热的热化学方程式(2分)。将燃烧产物通入BaCl2和HNO3的混合溶液,生成白色沉淀并放出无色气体,请用一个离子方程式表示该反应(2 分)。
(4) 写出一个由以上元素构成的1Oe-微粒与18e-微粒反应的离子方程式:
(2分)及其他合理答案。
如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充人lmdA、3molB,此时两容器体积均为500mL,温度为T0C保持温度不变发生反应:

(1) 下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是__ __(2分,全才得分)。
A.混合气体的总质量不随时间改变B 2V正(C)=3V逆(B)
C. A、B转化率相等D.物质D的质量不随时间改变
(2) 2minn后甲容器中反应达到平衡,测得C的浓度为2mol/L,此时容器的体积为____(2分)mL,B的转
化率a甲(B)为____ (2分)。
(3) 乙容器中反应达到平衡所需要的时间____2min(2分)(填“>”、“<”或“=”,下同),B的转化率a乙(B)为___ a甲(B) (2分)。
(4) 其它条件不变,甲中如果从逆反应方向开始建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加人C的物质的量n(C)为____ (2分)mol,加人D的物质的量n(D)应该满足的条件为(2分)。
现有X.Y.Z.W四种常见的含氧酸,其成酸元素分属周期表中短周期的第ⅣA族到第ⅦA。将四种含氧酸溶液分别进行光照或微热测得如下数据(其中Q为不确定的物质):
| 含氧酸 |
X |
Y |
Z |
W |
| 含氧酸质量/g |
25.2 |
a |
3.1 |
10.5 |
| 生成物U/g |
3.2 |
/ |
/ |
3.2 |
| 生成物V/g |
3.6 |
0.9 |
0.9 |
/ |
| 生成物Q/g |
18.4 |
3.2 |
b |
c |
根据中学所学知识回答下列问题:
(1)上表中含氧酸名称:Z,W,生成物名称:U,V。
(2)上表中数据:a为,b为,c为。
(3)将X的稀溶液加入Y中,反应的离子方程式是。
(4)对W的水溶液光照一段时间后,溶液的pH(填“增大”.“减小”或“不变”)。
W.X.Y.Z均为短周期主族元素,W的最外层电子数与核外电子总数之比为3:8;X的核外电子总数与Y的最外层电子数相等,X的原子序数是Z的原子序数的一半;W.Y.Z位于同一周期。
(1)W的单质是一种色晶体。
(2)W.Y.Z三种元素的气态氢化物稳定性由高到低的顺序是(用化学式表示,Z的气态氢化物与其同主族元素气态氢化物化学式写法相似)。
(3)用化学方程式证明元素原子的得电子能力Y强于W
(4)Y的最高价氧化物为无色液体,0.25mol该物 质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式。
质与一定量水混合得到一种稀溶液,并放出QkJ的热量,写出该反应的热化学方程式。
(5)已知A.B.C.D四种物质存在如下反应关系: A+B C+D
C+D
①若A是Y和Z常见价态的化合物,B是X的氢化物,D是Y的氢化物,反应过程中没有化合价变化,该反应的化学方程式是。
②若A是Z的单质,B为红色固体,D为紫红色固体单质,高温下发生该反应,C的化学式是。D与X元素最高价氧化物对应水化物的浓溶液反应,生成的气体会对大气造成污染。用烧碱溶液吸收该气体生成两种盐,其中一种盐可用作防腐剂,烧碱溶液吸收气体的离子方程式是。