现有X.Y.Z.W四种常见的含氧酸,其成酸元素分属周期表中短周期的第ⅣA族到第ⅦA。将四种含氧酸溶液分别进行光照或微热测得如下数据(其中Q为不确定的物质):
| 含氧酸 |
X |
Y |
Z |
W |
| 含氧酸质量/g |
25.2 |
a |
3.1 |
10.5 |
| 生成物U/g |
3.2 |
/ |
/ |
3.2 |
| 生成物V/g |
3.6 |
0.9 |
0.9 |
/ |
| 生成物Q/g |
18.4 |
3.2 |
b |
c |
根据中学所学知识回答下列问题:
(1)上表中含氧酸名称:Z ,W ,生成物名称:U ,V 。
(2)上表中数据:a为 ,b为 ,c为 。
(3)将X的稀溶液加入Y中,反应的离子方程式是 。
(4)对W的水溶液光照一段时间后,溶液的pH (填“增大”.“减小”或“不变”)。
[物质结构与性质]下列反应曾用于检测司机是否酒后驾驶:
2Cr2O72-+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为_______ __;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是________(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型为___________;1molCH3COOH分子中含有δ键的数目为 _____ _。
(3)与H2O互为等电子体的一种阳离子为_____ ___(填化学式);H2O与CH3CH3OH可以任意比例互溶,除因为它们都是极性分子外,还因为_____ ___。
FeCl3具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。请回答下列问题:
(1)FeCl3净水的原理是 。FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示) 。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(Cl-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
②完成NaClO3氧化FeCl2的离子方程式: ClO3-+
ClO3-+ Fe2++
Fe2++ =
= Cl-+
Cl-+ Fe3++
Fe3++ .
.
(3)FeCl3在溶液中分三步水解:
Fe3++H2O  Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)++H2O Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是 。
通过控制条件,以上水解产物聚合,生成聚合氧化铁,离子方程式为:
xFe3++yH2O Fex(OH)y(3x-y)++yH+
Fex(OH)y(3x-y)++yH+
欲使平衡正向移动可采用的方法是(填序号) 。
a.降温 b.加水稀释c.加入NH4Cl d.加入NaHCO3
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是 。
(4)天津某污水处理厂用氯化铁净化污水的结果如下图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为 mg·L-1。
(12分)研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。利用反应6NO2+ 8NH3 7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
7N5+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是 L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH="-196.6" kJ·mol-1
2SO3(g) ΔH="-196.6" kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH="-113.0" kJ·mol-1
2NO2(g) ΔH="-113.0" kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH= kJ·mol-1。
SO3(g)+NO(g)的ΔH= kJ·mol-1。
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是 。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 molNO2
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如下图所示。该反应ΔH 0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是 。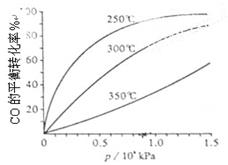
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,用ClO2替代Cl2对自来水进行消毒是城市饮用水处理新技术。工业上制备ClO2的方法很多,可以用合适的还原剂还原NaClO3制得。
(1)在硫酸酸化的条件下用 草酸还原NaClO3制ClO2,其反应的化学方程式为 。
(2)工业以CH3OH与NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体,已知该反应分为两步进行,第一步为2ClO3-+2Cl-+4H+=2ClO2↑+Cl2↑+2H2O。
①写出第二步反应的离子方程式 。
②工业生产时需在反应物中加少量Cl-,其作用是 。
(3)ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐,写出ClO2与NaOH溶液反应的离子方程式 。
(4)ClO2可用于含CN-废水的处理,产生的两种气体可以直接排入空气。
①已知CN-中C、N的最外层都满足8电子结构,写出CN-的电子式 。
②写出该反应的离子方程式 。
某品牌奶粉被鉴定为所含亚硝酸盐残留量高出正常值7. 8倍,长期食用可能致癌。NaNO2有像食盐一样的咸味,能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O。
(1)上述反应中若有1.75 mol的还原剂被氧化,则被还原的氧化剂是_________mol。
(2)某厂废切削液中,含2%~5%的NaNO2,直接排放会造成污染,下列试剂_________能使NaNO2转化为不引起二次污染的N2。(填编号)①NaCl ②NH4Cl ③H2O2 ④浓H2SO4
反应的化学方程式为___________________。若此废水呈强碱性,需调节溶液的pH接近中性,再添加氯化铵溶液,否则会引起二次污染,反应的方程式为______________________。
(3)向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸。下列离子方程式与事实不相符的是
| A.OH―+CO32―+2H+→HCO3―+H2O |
| B.2OH―+CO32―+3H+→HCO3―+2H2O |
| C.2OH―+CO32―+4H+→CO2↑+3H2O |
| D.OH―+CO32―+3H+→CO2↑+2H2O |