现有3瓶没有标签的无色溶液,它们分别是NaHCO3、Ba(OH)2、H2SO4
中的各一种,某研究性学习小组探究“不用其它试剂即可鉴别”的方法。将试剂瓶分别编号为①、②、③。
⑴甲同学采用如下实验方案:
分别取样进行分组实验,现象如下表所示:
| |
③ |
② |
① |
| ① |
↑ |
↓ |
|
| ② |
↓ |
|
↓ |
| ③ |
|
↓ |
↑ |
根据实验现象得出结论:②试剂为 。
甲同学又做如下两个实验,鉴别①和③
请分析甲同学实验失败的可能原因: 。
⑵乙同学采用如下实验方案:
乙同学采用甲同学同样的实验过程,鉴别出其中的②后,又做如下实验:
请分析乙同学实验失败的可能原因: 。
⑶丙同学采用如下实验方案:
丙同学采用甲同学同样的实验过程,鉴别出其中的②后,又做如下实验: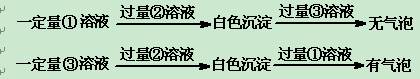
根据实验现象得出结论:①试剂为 ,③试剂为 。
⑷丁同学参与甲、乙、丙三位同学的实验过程,发现当采用分组实验鉴别出②后,无需再进行任何实验操作,立即就可区分出另外两瓶试剂,他的方法是 。
为检验炭粉与浓硫酸反应的产物设计如下装置,回答相关问题: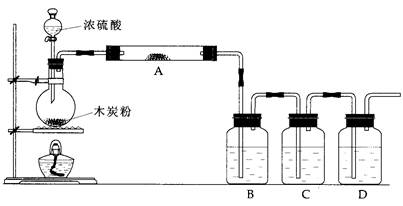
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用
A中加入的试剂和作用是______ _____
B中加入的试剂和作用是____ ____________
D中加入的试剂和作用是__ ___________
(4)实验时,C中应观察到的现象是______________________
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·l-1 NaOH溶液。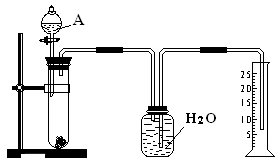
请填写下列空白
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。正确的操作顺序是
(2)A中可选用的溶液是
(3)实验中发生反应的化学方程式为
(4)若实验中测得样品的质量为W g ,氢气的体积为aL (标准状况),则样品中Al的质量分数为
在实验室中严禁打闹,某几个同学在做实验中打闹而同时把盛有浓盐酸和盛固体KClO3的试剂瓶打破,使其在地上混合立即产生大量黄绿色气体,发生反应的化学方程式为:KClO3+ 6HCl(浓) KCl+3Cl2↑ + 3 H2O
KCl+3Cl2↑ + 3 H2O
(1)该反应中的氧化剂是___________。
(2)在化学方程式上标出电子转移的方向和数目。
(3)如反应中转移了0.50 mol电子,则产生的气体在标准状况下体积为________ L 。
(4)在清除碎片时某同学用湿毛巾捂住鼻子防止中毒,有以下四种溶液可浸湿毛巾,它们分别是:①NaOH溶液②NaCl溶液③KBr溶液④NaHCO3溶液. 正确选择是(填试剂号数).
有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO、Cl-、NO等离子中的若干种。现做如下实验:
(1)取少量该溶液,滴入用硝酸酸化的AgNO 3溶液,有白色沉淀生成。
(2)另取部分溶液,加入氢氧化钠,有白色沉淀产生,加入氢氧化钠的量与生成白色沉淀的量可用下图表示。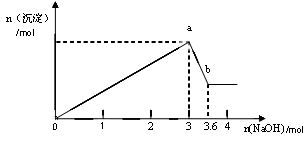
试推断:
(1)该溶液中一定存在______________,一定不存在________________。
(2)上述溶液中至少有__________、_________(填化学式)等物质混合而成;其物质的量比为。
(3) 写出图中a b变化过程的离子方程式。
b变化过程的离子方程式。
科学探究结果的准确性来自于探究活动中研究方法的科学性,研究过程的计划性、研究目的明确性。
(一)学生(甲)应用下图装置(A)所示意的方法研究氯气的性质,其中气体的主要成分是氯气(含有空气和水蒸气)。请回答下列问题: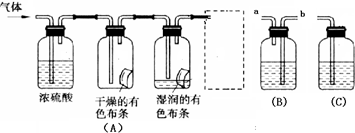
(1)该项研究(实验)的主要目的是
(2)浓硫酸的作用是。与研究目的直接相关的实验现象是 ________________ _。
(3)虚框中的装置应选择(填“B”或“C”),其盛放的试剂
为(填试剂名称);使用该装置的目的是;该装置内发生反应的化学方程式为。
(二)学生(乙)设计实验探究金属铝表面氧化膜的性质:将铝片(含氧化膜)投入浓氯化铜溶液中,铝表面很快出现一层海绵状暗红色物质。若用同样的铝片投入同浓度的硫酸铜溶液中,在短时间内铝片无明显变化。回答下列问题:
(1)铝片表面出现的暗红色物质的过程中发生的离子反应方程式是。
(2)同学(乙)认为:铝与氯化铜溶液能迅速反应,而与同浓度的硫酸铜溶液在短时间内不反应的原因是“氯离子能破坏氧化铝表面薄膜,而硫酸根离子不能”。并设计如下实验方案进行验证,请你根据其思路完成下列空格:
[实验方案] 在硫酸铜溶液中加入铝片,无明显现象,再加入(填试剂名称),若反应明显加快了,说明上述推断正确。