丁基橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体的分子式为,氢化后得到2-甲基丙烷。
完成下列填空:
1)可以聚合,写出的两种聚合方式(以反应方程式表示)。
2)与某烷发生烷基化反应生成分子式为的物质,的一卤代物只有4种,且碳链不对称。写出的结构简式。
3)写出将通入下列两种溶液后出现的现象。
通入溴水:
通入溴的四氯化碳溶液:
4)烯烃和作用,烯烃中与双键碳相邻碳原子上的一个氢原子被溴原子取代。分子式为的烃和作用,得到的一溴代烯烃有种。
下图是在实验室进行氨气快速制备与性质实验的组合装置,部分固定装置未画出。
(1)在组装好装置后,若要检验A~E装置的气密性,其操作是首先____ ,然后微热A,观察到E中有气泡冒出,移开酒精灯或松开双手,E中导管有水柱形成,说明装置气密性良好。
(2)装置B中盛放的试剂是________,装置D的作用是
(3)点燃C处酒精灯,关闭弹簧夹2,打开弹簧夹l,从分液漏斗放出浓氨水至浸没烧瓶中固体后关闭分液漏斗,稍候片刻,装置C中黑色固体逐渐变红,装置E中溶液里出现大量气泡,同时还可能产生的现象是________;从E中逸出液面的气体可以直接排入空气,请写出在C中发生反应的化学方程式:________。
(4)当C中固体全部变红色后,关闭弹簧夹1,慢慢移开酒精灯,待冷却后,称量C中固体质量,若反应前固体质量为16 g,反应后称重固体质量减少2.4 g,通过计算确定该固体产物的成分是________(用化学式表示)。
(5)在关闭弹簧夹1后,打开弹簧夹2,残余气体进入F中,很快发现装置F中产生白烟,同时发现G中溶液迅速倒吸流入F中。请写出产生白烟的化学方程式:________,迅速产生倒吸的原因是________。
草酸晶体的组成可表示为H2C2O4·xH2O。实验室常用其加热分解制取CO气体,反应方程式为:H2C2O4·xH2O  CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。
CO+CO2+(x+1)H2O。下图为分解草酸晶体,用干燥纯净的CO还原CuO制取Cu,并收集CO的实验装置(略去铁架台、铁夹等支撑加持装置),回答下列问题。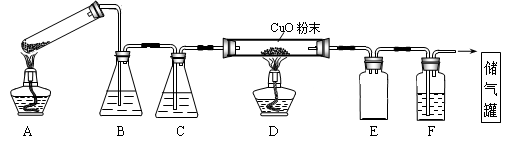
(1)A装置为加热分解草酸的装置,该装置错误是______________,C装置中盛放的试剂是______ _ ,E装置的作用是__________ 。
(2)实验过程中涉及到如下操作:①点燃A处的酒精灯 ②熄灭A处的酒精灯 ③点燃D处的酒精灯 ④熄灭D处的酒精灯。这4步操作由先到后的顺序为________ (填序号)。点燃D处酒精灯前必须要进行的操作名称是__________。
(3)用酸性高锰酸钾溶液滴定草酸晶体,求x的值。
实验步骤:准确称取1.26g 草酸晶体,配成100mL溶液;取出20.00mL于锥形瓶中,再向瓶中加入足量稀H2SO4;用0.0500mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液16.00mL。滴定时,所发生的反应为:
2MnO4-+5H2C2O4+6H+ = 10CO2+2Mn2++8H2O。
①配制草酸溶液除需要玻璃棒、烧杯,还一定需要的玻璃仪器有_____________。
② x=________。
某实验小组同学依据资料深入探究Fe3+在水溶液中的行为。
资料:
i.Fe3+在水溶液中以水合铁离子的形式存在,如[Fe(H2O)6]3+;
[Fe(H2O)6]3+发生如下水解反应:
[Fe(H2O)6]3+(几乎无色) + nH2O  [Fe(H2O)6-n(OH)n]3-n(黄色) + nH3O+(n = 0~6) ;
[Fe(H2O)6-n(OH)n]3-n(黄色) + nH3O+(n = 0~6) ;
ii.[FeCl4(H2O)2]-为黄色。
进行实验:
【实验I】
【实验II】
分别用试管①、③中的试剂作为待测液,用色度计测定其透光率。透光率越小,溶液颜色越深;透光率越大,溶液颜色越浅。

图1图2
Fe(NO3)3溶液透光率随温度变化曲线FeCl3溶液透光率随温度变化曲线
(1)实验I中,试管②溶液变为无色的原因是 。
(2)实验I中,试管③溶液呈棕黄色与[FeCl4(H2O)2]-有关,支持此结论的实验现象是 。
(3)由实验II图1、2可知:加热时,溶液颜色 (填“变浅”、“变深”或“不变”)。
(4)由实验II,可以得出如下结论:
[结论一] FeCl3溶液中存在可逆反应:[FeCl4(H2O)2]- + 4H2O  [Fe(H2O)6]3+ + 4Cl-,得出此结论的理由是 。
[Fe(H2O)6]3+ + 4Cl-,得出此结论的理由是 。
[结论二] 结论一中反应的ΔH (填“>0”或“<0”)。
(5)实验小组同学重新设计了一个实验证明(4)中结论一。实验方案:取试管①中溶液, (请描述必要的实验操作和现象)。
葡萄酒中抗氧化剂的残留量是以游离SO2的含量计算,我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。某兴趣小组设计实验方案对葡萄酒中SO2进行测定。
Ⅰ.定性实验方案如下:
(1)将SO2通入水中形成SO2 ─饱和H2SO3溶液体系,此体系中存在多个含硫元素的平衡,分别用平衡方程式表示为_______________。
(2)利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如下实验:
实验结论:干白葡萄酒不能使品红溶液褪色,原因为:_________________________。
Ⅱ.定量实验方案如下(部分装置和操作略):
(3)仪器A的名称是________________。
(4)A中加入100.0mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为______________。
(5)除去B中过量的H2O2,然后再用NaOH标准溶液进行滴定, 除去H2O2的方法是__________。
(6)步骤X滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2的含量为__________g/L。该测定结果比实际值偏高,分析原因________________________。
乙酰苯胺为无色晶体,有“退热冰”之称。其制备原理为:
已知:①苯胺易被氧化;②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
| 试剂名称 |
熔点℃ |
沸点℃ |
溶解度(20 ℃) |
| 苯胺 |
-6.2 |
184.4 |
稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 |
16.7 |
118 |
易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 |
114~116 |
280~290 |
0.46g |
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。
图1图2
(1)仪器a的名称为 。
(2)步骤1中加入锌粉的作用是 。
(3)步骤2中控制温度计示数约105 ℃的原因是 。
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是 ,当过滤的溶液具有强酸性、强碱性或强氧化性时要用 代替布氏漏斗,停止抽滤时的操作为 。