黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验: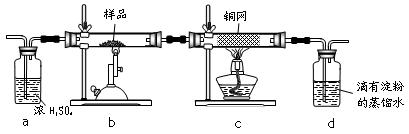
现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的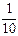 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,终读数如图所示。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,终读数如图所示。请回答下列问题: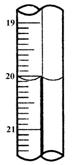
(1)称量样品所用的仪器为_____,将样品研细后再反应,其目的是_______。
(2)装置A的作用是________。
a.有利于空气中氧气充分反应 b.除去空气中的水蒸气
c.有利于气体混合 d.有利于观察空气流速
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)滴定时,标准碘溶液所耗体积为_________mL。
判断滴定已达终点的现象是_______。
通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____。(填编号)
(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。
过氧 化氢对环境友好,性质多样,有很重要的研究和应用价值。
化氢对环境友好,性质多样,有很重要的研究和应用价值。
(1)实验室利用反应 可制备氧气。
可制备氧气。
①取等物质的量浓度等体积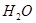
 溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
| 序号] |
条件 |
现象 |
结论 |
|
| 温度/℃ |
催化剂 |
|||
| 1 |
40 |
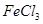 溶液 溶液 |
||
| 2 |
20 |
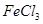 溶液 溶液 |
||
| 3 |
20 |
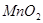 |
||
| 4 |
20 |
无 |
实验1、2研究的是______________对 分解速率的影响。
分解速率的影响。
实验2、3的目的是____________________________。
实验中可以表明该反应速率差异的现象是______________。
②实验室用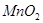 做该反应的催化剂,使用如下图所示装置的A部分制备
做该反应的催化剂,使用如下图所示装置的A部分制备 ,避免反应过于剧烈的操作是______________。
,避免反应过于剧烈的操作是______________。
(2) 与水反应也可生成
与水反应也可生成 ,某同学取
,某同学取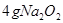 样品与过量水反应,待反应完全终止时,得
样品与过量水反应,待反应完全终止时,得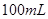 溶液X和
溶液X和 (已折算为标准状况),该同学推测样品中含有杂质或反应中生成
(已折算为标准状况),该同学推测样品中含有杂质或反应中生成 ,并进行实验研究。
,并进行实验研究。
①取少量X于试管中,滴加 溶液,立即生成红褐色沉淀,则反应的离子方程式为________________________________________________________。
溶液,立即生成红褐色沉淀,则反应的离子方程式为________________________________________________________。
②通过如上图所示整套实验装置测定 样品的纯度,假设所含杂质不参加反应,取25
样品的纯度,假设所含杂质不参加反应,取25 ,滴入烧瓶内使其与过量
,滴入烧瓶内使其与过量 酸性溶液反应,最终生成
酸性溶液反应,最终生成 (已折算为标准状况),则此样品中
(已折算为标准状况),则此样品中 的质量分数是____________________________。
的质量分数是____________________________。
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ ________。直到因加入一滴盐酸后,溶液由黄色变为橙色,并_______________为止。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________
| A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 |
| B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为_________mL,终点读数为_____________mL;所用盐酸溶液的体积为______________ mL。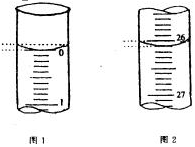
(4)某学生根据三次实验分别记录有关数据如下表: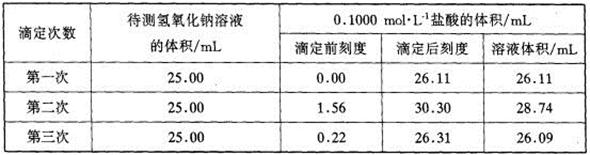 请用上述数据列式计算该氢氧化钠溶液的物质的量浓度。
请用上述数据列式计算该氢氧化钠溶液的物质的量浓度。
下图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的装置图,请回答下列问题: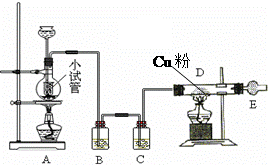
⑴ 小试管的作用是;烧瓶中发生反应的化学方程式是;
⑵ B瓶中的溶液是,其作用是;C瓶中盛放的溶液是,其作用是。
⑶ 玻璃管D中反应的现象是。
⑷ 干燥管E中盛有碱石灰,其作用是。
⑸ 开始实验时,应先点燃处(填“A”或“D” )的酒精灯,当时再点燃另一处的酒精灯。
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。根据所学知识,回答下列问题:
⑴工业上将氯气通入石灰乳制取漂白粉,反应的化学反应方程式为;漂白粉有效成分为(填名称);瓶装漂白粉久置空气中会呈稀粥状而失效,试用化学方程式表示失效的原因。
(2)某化学兴趣小组为了探究HClO的漂白性,设计了如下的实验。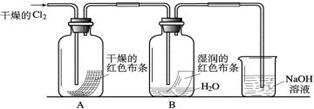
a.通入Cl2后,从集气瓶A、B的现象可得出的结论是;其中发生的反应的化学方程式为。
b.为了确认是HClO使湿润的红色布条褪色,你认为还应增加的实验是。
c.烧杯中溶液所起的作用是,烧杯中所发生反应的化学方程式为。
d.为保证实验安全,氯气以每分钟1.12L(已换算为标准状况下)的流速匀速通入,若实验需耗时4分钟,小烧杯中盛放2 mol·L—1的NaOH溶液的体积至少应为 mL。
mL。
现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL、0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)。
(2)经计算,需浓H 2SO4的体积为。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是。(填序号)
2SO4的体积为。现有①10 mL ②50 mL ③100 mL三种规格的量筒,你选用的量筒是。(填序号)
(3)将浓H2SO4加适量蒸馏水稀释后,冷却片刻,随后全部转移到mL的容量瓶中,转移时应用玻璃棒。转移完毕,用少量蒸馏水洗涤2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水注入容量瓶直到液面接近刻度处。改用滴加蒸馏水到瓶颈刻度的地方。振荡摇匀后,装瓶贴签。
(4)在配制过程中,其他操作都准确,下列操作中错误的是(填序号,以下同),能引起误差偏高的有。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线