有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸中,A极为负极;②C、D用导线相连后,同时浸入稀硫酸中,电流由D→导线→C;③B、C相连后,同时浸入稀硫酸中,C极产生大量气泡;④B、D相连后,同时浸入稀硫酸中,D极产生大量气泡。据此,判断四种金属的活动性顺序是
A. A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>D>C>A
某同学设计了如下实验方案用以检验淀粉水解的情况: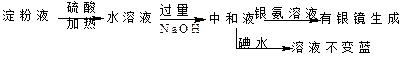
下列结论正确的是 ( )
| A.淀粉尚有部分未水解 | B.淀粉已经完全水解 |
| C.淀粉没有水解 | D.淀粉已经发生水解,但不知是否完全水解 |
下列实验可达到实验目的的是()
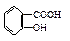 ①.将与NaOH的醇溶液共热制备CH3—CH═CH2
①.将与NaOH的醇溶液共热制备CH3—CH═CH2
②.乙酰水扬酸与适量NaOH溶液反应制备
③.向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④.用溴的四氯化碳溶液吸收SO2气体
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |
某胶体遇盐卤或石膏水易发生了聚沉,而遇食盐水或硫酸钠溶液不易发生聚沉。下列有关说法正确的是 ( )
| A.胶体直径为10-9~10-7cm |
| B.此胶体的胶粒带正电荷 |
| C.遇BaCl2溶液或Fe(OH)3胶体可发生聚沉 |
| D.Na+使此胶体聚沉的效果比Ca2+、Mg2+好 |
设计实验证明亚硫酸既有氧化性又有还原性,必选试剂是 ( )
| A.盐酸、浓硫酸、氯化钡溶液 | B.溴水、硫化钠溶液、稀硫酸 |
| C.硝酸、硫化氢、氢氧化钠溶液 | D.氧气、氯化钡溶液、水 |
使a g Fe粉与一定量的硝酸溶液充分反应(Fe粉完全溶解),生成的气体与标准状况下b L O2混合后,恰好能被水完全吸收,a和b的关系可能是()
A.b>0.3a B. b<0.2a c. 0.2a<b<0.3aD.0.2a≤b≤0.3a