(1)在洁净的试管中加入少量硝酸银溶液,再逐滴滴加稀氨水,现象是先生成白色沉淀,反应的离子方程式是①______________________________ ;继续滴加至沉淀恰好溶解,即得银氨溶液,反应的离子方程式为②_______________________________________;
(2)葡萄糖分子中含有醛基,属于多羟基醛,工业上常用来制镜。向(1)中所得的银氨溶液中滴入少量葡萄糖溶液,混合均匀后,放在水浴中加热3min~5min,即可在试管内壁上形成银镜,则此反应的化学方程式为③(葡萄糖的结构简式用GCHO表示):____________________________________________________。
某高分子材料的结构如右图,则其对应的单体的结构简式为:______________________,______________________。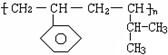
组成一种原电池如图所示。试回答下列问题(灯泡功率合适):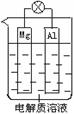
(1)电解质溶液为稀H2SO4时,灯泡______(填“亮”做①题,填“不亮”做②题) 。
。
①若灯泡亮,则Mg电极上发生的反应为:____________________;
Al电极上发生的反应为:___________________________________。
②若灯泡不亮,其理由为:__________________________________。
(2)电解质溶液为NaOH溶液时,灯泡_____(填“亮”做①题,填“不亮”做②题)。
①若灯泡亮,则Al电极上发生的反应为:_____________________________。
②若灯泡不亮,其理由为:__________________________________________。
已知A是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。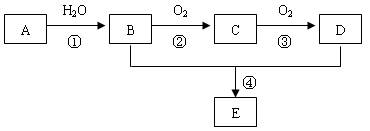
请回答下列问题:
(1)写出A的结构简式。
(2)B、D分子中的官能团名称分别是、。
(3)物质B可以被直接氧化为D,需要加入的试剂是。
(4)写出下列反应的化学方程式:
①;反应类型:。
④。反应类型:。
某烷烃的蒸气质量是相同条件下氢气质量的36倍,该烃的分子式为____________,写出该烃同分异构体的结构简式:
在盛有少量无水乙醇的试管中,加入一小块新切的、擦干表面煤油的金属钠,迅速用配有导管的单孔塞塞住试管口,用一小试管收集并验纯气体后,点燃,并把干燥的小烧杯罩在火焰上,,片刻,迅速倒转烧杯,向烧杯中加入少量澄清石灰水。观察现象,完成下表。
| 乙醇与钠反应的现象 |
气体燃烧的现象 |
检验产物 |
| 气体燃烧时火焰呈, 小烧杯内壁, 澄清石灰水。 |
反应中只生成了 |
写出乙醇与钠反应的化学方程式