(1)氢氧化铝Al(OH)3是一种治疗胃酸(含盐酸)过多的药物,请用化学方程式 表示该反应的原理: 。
表示该反应的原理: 。
(2)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,主要是因为上述两种物质发生了某种反应,请用化学方程式表示该反应的原理:
。
(3 )醋还可用于除去热水瓶胆内的水垢(设其主要成分为碳酸钙),请用化学方程式表示该反应的原理: 。
)醋还可用于除去热水瓶胆内的水垢(设其主要成分为碳酸钙),请用化学方程式表示该反应的原理: 。
煤作为燃料,可以有下列两种途径(把煤看成由碳组成):
途径Ⅰ:C(s)+O2(g)===CO2(g) ΔH=-a kJ·mol-1
途径Ⅱ:C(s)+H2O(g)===CO(g)+H2(g) ΔH=+b kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-c kJ·mol-12H2(g)+O2(g)===2H2O(g) ΔH=-d kJ·mol-1
试回答下列问题:
(1)燃烧等质量的煤,途径Ⅰ放出的热量____途径Ⅱ放出的热量(填“大于”、“小于”或“等于”)。
(2)b的数学关系式是______________(用a、c、d表示)。
(3)由于制取水煤气反应中,反应物具有的总能量________(填“大于”、“小于”或“等于”)生成物所具有的总能量,在反应时,反应物需要______(填“吸收”或“放出”)能量才能转化为生成物。
(4)简述煤通过途径Ⅱ作为燃料的意义__________________________________________________。
Ⅰ.已知某反应A(g)+B(g)  C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
C (g)+D(g),过程中的能量变化如图所示,回答下列问题。
(1)该反应是______________反应(填“吸热”或“放热”),该反应的ΔH=____________kJ·mol-1(用含E1、E2的代数式表示),1 mol气体A和1 mol气体B具有的总能量比1 mol气体C和1 mol气体D具有的总能量____________(填“一定高”、“一定低”或“高低不一定”)。
(2)若在反应体系中加入催化剂使逆反应速率增大,则E1和E2的变化是:E1______,E2_________,ΔH_________(填“增大”“减小”或“不变”)。
Ⅱ.已知下列热化学方程式
Fe2O3(s)+3CO(g) ===2Fe(s)+3CO2(g)ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g)ΔH2=-47 kJ·mol-1②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g)ΔH3=+19 kJ·mol-1③
写出FeO(s)被CO还原成Fe和CO2的热化学方程式_______________________________________。
有一化学反应2A  B+D ,B、D起始浓度为0,在三种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
B+D ,B、D起始浓度为0,在三种不同条件下进行。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表,根据下述数据,完成填空:
(1)在实验1,反应在0至20分钟时间内A的平均速率为_______mol/(L·min)。
(2)在实验2,A的初始浓度C2=____________mol/L,可推测实验2中隐含的条件是___________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则达到平衡时v3v1(填>、=、<=,)800℃时,反应平衡常数=,且C3=_______mol/L,可推测实验3中隐含的条件是___________。
(4)800℃时,反应B+D  2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0, 达到平衡时A的浓度为mol/L, B的转化率=。
2A当其他条件不变, B、D的起始浓度为0.50 mol/L , A的起始浓度为0, 达到平衡时A的浓度为mol/L, B的转化率=。
在如图所示的三个容积相同的三个容器①、②、③进行如下的反应:3A(g)+B(g) 2C(g)△H<0
2C(g)△H<0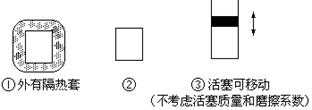
(1)若起始温度相同,分别向三个容器中充入3mol A和1mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为(填容器编号)
(2)若维持温度不变,起始时②中投入3mol A、1mol B; ③中投入3mol A、1mol B和2mol C,则达到平衡时,两容器中B的转化率②③(填<、>或=)
(3)若维持②③容器内温度和压强相等,起始时在②中投入3molA和1molB,在③中投入amol A和bmol B及cmol C,欲使达平衡时两容器内C的百分含量相等,则两容器中起始投料量必须满足(用含a、b、c的关系式表达):
食盐是日常生活的必需品,也是重要的化工原料。用提纯的NaCl配制250mL 2.00 mol·L-1 NaCl溶液。
①所用定容仪器的名称和规格为。
②计算后,需称出NaCl质量为___________g。
③下列操作的正确顺序是(用字母表示) B→ → → → → →G 。
A摇匀 B.称量 C.洗涤 D.定容 E.溶解 F.移液 G.装瓶
④下列操作对所得溶液浓度有何影响, 在横线上填写“偏高”“偏低”或“无影响”。
A 定容时仰视容量瓶刻度线:。B 称量时砝码生锈:。