为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色的浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须除去之,再与溴水反应。
请你回答下列问题:
(1)甲同学设计的实验_______(填“能”或“不能”)验证乙炔与溴发生加成反应,其理由是_______。
a.使溴水褪色的反应,未必是加成反应
b.使溴水褪色的反应,就是加成反应
c.使溴水褪色的物质,未必是乙炔
d.使溴水褪色的物质,就是乙炔
(2)乙同学推测此乙炔中必定含有一种杂质气体是_______,它与溴水反应的化学方程式是_______;在验证过程中必须全部除去。
(3)请你选用图2-2所列四个装置(可重复使用)试验乙同学的实验方案,将它们的编号填入方框,并在括号中写出装置内所放的化学药品。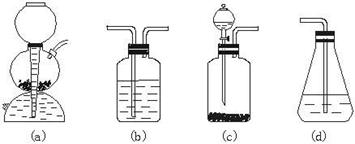

图2-2
(4)为验证这一反应是加成而不是取代反应,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是_______。
有机化合物F是合成电子薄膜材料高聚物Z和增塑剂P的重要原料。
(1)某同学设计了由乙烯合成高聚物Z的3条路线(I、II、III)如下图所示。
① 3条合成路线中,你认为符合“原子经济”要求的合成路线是(填序号“I”、 “II”或“III”)。
② X的结构简式是。
③ l mol F在 中充分燃烧,生成
中充分燃烧,生成 和
和 的物质的量之比为8:3,消耗7.5mol
的物质的量之比为8:3,消耗7.5mol ,其核磁共振氢谱中有3个吸收峰,且能与
,其核磁共振氢谱中有3个吸收峰,且能与 反应生成
反应生成 。
。
F分子中含有的含氧官能团的名称是。
Y+F Z反应的化学方程式是。
Z反应的化学方程式是。 (
( 、
、 代表烃基或氢原子)
代表烃基或氢原子)
合成P的路线如下图所示。D分子中有8个碳原子,其主链上有6个碳原子,且分子内只含有两个 。
。
① A B反应的化学方程式是。
B反应的化学方程式是。
② B C的反应中,B分子在加热条件下脱去一个水分子,生成C;C分子中只有1个碳原子上无氯原子。C的结构简式是。
C的反应中,B分子在加热条件下脱去一个水分子,生成C;C分子中只有1个碳原子上无氯原子。C的结构简式是。
③ P的结构简式是。
④符合下列条件的B的同分异构体共有(填数字)种。
a.在酸性条件下水解为M和N b.一定条件下M可以转化为N
⑤已知: (R代表烃基或氢原子)
(R代表烃基或氢原子)
A的同系物W的相对分子质量为44。请参照示例写出以W和另一种有机物为原料合成肉桂醇(
 )的合成路线:
)的合成路线: 。
。


甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。甲+乙 丙+丁
丙+丁
(1)转化关系中所涉及的反应为非氧化还原反应,且乙为水。
①若甲为块状固体,丙为可燃性气体,其分子内既含有极性键又含有非极性键。则丙的电子式是。
②若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示,丙具有漂白性。则甲中Cl元素的化合价是。
(2)转化关系中所涉及的反应为氧化还原反应,且乙为水。
①若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是。
②若丙和丁都可在一定条件下还原 ,此反应的化学方程式是。
,此反应的化学方程式是。
③若甲是由N和O元素组成的气态物质,呈红棕色。将3.36 g 加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是。
加到一定量丙溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是。
(3)Hofmann依据上述转化关系测定氨分子的组成。现用如右图所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至 处。
处。
①滴下浓氨水一段时间后,试管内发生反应的化学方程式是。
②证明试管内“不再反应”的实验操作和现象是。
(10分)工业上以锂辉石( ,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
已知:①
②某些物质的溶解度( )如下表所示。
)如下表所示。
| T/℃ |
20 |
40 |
60 |
80 |
| S(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
| S(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣1中分离出A12O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤II中反应的离子方程式是。
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
①a中,阳极的电极反应式是。
②b中,生成Li2CO3反应的化学方程式是。
(14分)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值。
(1)实验室利用反应 可制备氧气。
可制备氧气。
①取等物质的量浓度等体积 溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
| 序号 |
条件 |
现象 |
结论 |
|
| 1 |
温度/℃ |
催化剂 |
||
| 2 |
40 |
FeCl3溶液 |
||
| 3 |
20 |
FeCl3溶液 |
||
| 4 |
20 |
MnO2 |
||
| 5 |
20 |
无 |
实验1、2研究的是对H2O2分解速率的影响。
实验2、3的目的是。
实验中可以表明该反应速率差异的现象是。
②实验室用 MnO2做该反应的催化剂,使用如右图所示装置的A部分制备O2,避免反应过于剧烈的操作是。
MnO2做该反应的催化剂,使用如右图所示装置的A部分制备O2,避免反应过于剧烈的操作是。
(2)Na2O2与水反应也可生成O2。某同学取4 g Na2O2样品与过量水反应,待反应完全终止时,得100 mL溶液X和448 mL O2(已折算为标准状况)。该同学推测样品中含有杂质或反应中生成H2O2,并进行实验研究。
①取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀。则反应的离子方程式是。
②通过如上图所示整套实验装置测定Na2O2样品的纯度,假设所含杂质不参加反应。取25 mL X,滴入烧瓶内使其与过量KMnO4酸性溶液反应,最终生成56 mL O2(已折算为标 准状况),则此样品中:Na2O2的质量分数是。
准状况),则此样品中:Na2O2的质量分数是。
为探究铁与浓硫酸在加热条件下的反应,某活动小组设计并完成以下实验:
(1)实验目的:分析铁与浓硫酸在加热条件下的反应。
①洗气瓶中浓硫酸的作用是。
②写出加热条件下铁与浓硫酸反应生成SO2的化学方程式。
活动小组预测随着反应的进行,硫酸的浓度降低,可能还会有氢气产生,为进一步确认气体的成分还需要进行进一步的实验。
(2)实验目的:检验气体的成分。
试剂:氢氧化钠溶液、浓硫酸、氧化铜粉末、无水硫酸铜固体、品红溶液、高锰酸钾酸性溶液、碱石灰。
仪器如下图(可重复使用,可根据需要取用);
①连接仪器。将装置的字母填入□内,并将试剂名称填写在相应的括号内(可不填满)
②若混合气体中含有氧气,实验过程中能观察到的现象是。
(3)实验目的:确定产物的含量。
①若混合气体中含有SO2和H2,为测定混合气体中各成分含量,需收集的数据有。
②若反应后烧瓶中溶液含有的金属阳离子有Fe2+、Fe3+,其中检验是否含有Fe3+可采用的试剂为;如果该过程中共消耗了11.2g铁,反应后的溶液能吸收标准状况下1.12L氯气,则原溶液中含有Fe3+的物质的量为mol。