、已知有机物A只由碳、氢两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平。一定条件下,A、B、C、D、E有如下转化关系: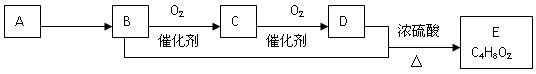
(已知:2RCHO+O2→2RCOOH)
(1)除去甲烷中混有A的试剂是 。
(2)请写出B→C的方程式 。
(3)请写出B与D反应生成E的化学方式 。
(4)某同学设计了下列反应: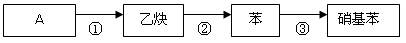
请写出③的反应方程式 。
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 |
Ag+ Na+ |
| 阴离子 |
NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。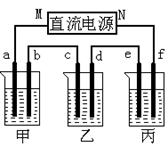
接通电源,经过一端时间后,测得乙中C电极质量增加了27克。常温下各烧杯中溶液的pH与电解时间t的关系图如下。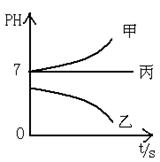
据此回答下列问题:
(1)M为电源的_______极(填写“正”或“负”),甲、乙电解质分别为_______、_______(填写化学式)。
(2)f电极的电极反应式为,生成的气体在标准状况下的体积为_____________。
(3)写出乙烧杯的电解池反应_____________________________。
(4)若电解后甲溶液的体积为25L,则该溶液的pH为___________ 。
(5)要使丙恢复到原来的状态,应加入_______ g 。(填写化学式)
硫酸亚锡(SnSO4)是一种重要的硫酸盐,广泛应用于镀锡工业。某研究小组设计SnSO4制备路线如下: 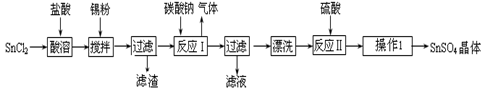
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成碱式氯化亚锡, Sn相对原子质量为119
回答下列问题:
(1)锡原子的核电荷数为50,锡元素在周期表中的位置是。
(2)操作Ⅰ是。
(3)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因。
(4)加入Sn粉的作用有两个:①调节溶液pH②。
(5)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子反应方程式是。
(6)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是。
(7)该小组通过下列方法测定所用锡粉的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl===SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2 + K2Cr2O7 + 14HCl ===6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1.226 g 锡粉,经上述各步反应后,共用去0.100 mol/L K2Cr2O7溶液32.0ml。锡粉中锡的质量分数是。
(1)硫化氢具有还原性,可以和许多氧化剂反应。H2S通入硫酸酸化的KMnO4溶液,反应生成S、MnSO4等,写出该反应的化学方程式:。
(2)硫铁矿氧化焙烧的化学反应如下: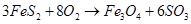
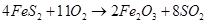
若24mol FeS2完全反应耗用氧气1467.2L(标准状况);反应产物中Fe3O4与Fe2O3物质的量之比为。
(3)在常温常压下氢气与氧气的混合气体10L,将混合气体点燃充分反应后恢复到原来状况剩余气体1L,则原混合气体中氢气和氧气的体积比为
(4)将钠—铝合金共a 克,投入足量水中生成气体最多mol,如果投入到足量的稀硫酸中生成气体体积最多mol(用含a的代数式表示,上同)
某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示。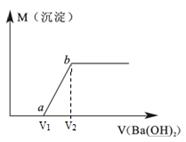
(1)该溶液中一定含。(填化学式)
(2)写出图中a点之前的离子方程式:
(3)将所得沉淀进行过滤,洗涤,干燥,称量,应如何判断沉淀是否完全洗净:。
(4)若b点时沉淀质量=2.94克,V1=20mL,V2=40mL,求C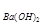 =。
=。
(1)写出下图中序号①~③仪器的名称:
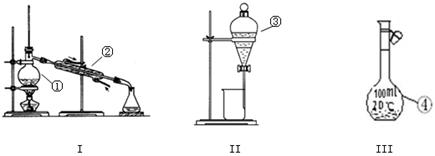
①;②;③。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(3)下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:①胶头滴管②烧瓶③烧杯④ 玻璃棒⑤药匙⑥量筒⑦托盘天平。
请回答下列问题:
a.该硫酸的物质的量浓度为mol· L-1。
b.配制稀硫酸时,还缺少的仪器有 (写仪器名称)。
c.经计算,配制480mL 1mol· L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为__mL。
d.对所配制的稀硫酸进行测定,发现其浓度大于1 mol· L-1,配制过程中下列各项操作可能引起该误差的原因有。
| A.定容时,俯视容量瓶刻度线进行定容 。 |
| B.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作。 |
| C.转移溶液时,不慎有少量溶液洒到容量瓶外面。 |
| D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 。 |
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处。