现有A、B、C、D四种短周期元素(零族除外),请根据信息回答下列问题。
| 元素 |
A |
B |
C |
D |
| 性质或结构信息 |
元素非金属性较强,其最高价氧化物对应的水化物为强酸,但其单质稳定,常作保护气。 |
原子核外电子占了4个轨道 |
原子半径仅比氢原子大,其氢化物溶于水形成弱酸 |
原子核外有5种不同能量的电子,且s电子数比p电子数少1个 |
(1)A元素原子的核外电子排布式为: 。
(2)写出C元素的单质与水反应的化学方程式 ;A、C两元素的氢化物的稳定性强弱是 > (用化学式表示)。
(3)D元素最高价氧化物对应的水化物呈 (选填“酸性”、“碱性”或“两性”)。
(4)B元素最简单的氢化物分子为 分子(选填“极性”或“非极性”)。4g该氢化物在空气中完全燃烧生成液态水时,放出222.575kJ热量,写出表示该氢化物燃烧热的热化学方程式 。
A、B、C、D分别为(NH4)2SO4、Ba(OH)2、AlCl3、Na2CO3 4种物质中的1种,现进行如下实验:
①实验测得A溶液和D溶液显碱性,B溶液和C溶液显酸性;
②A溶液和D溶液混合可生成沉淀甲
③足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体;
请回答:
(1)B的化学式为________;沉淀甲的化学式为________。
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为。
(3)加热蒸干C溶液并灼烧,最后所得固体为________(填化学式)。
(4)D溶液中各离子浓度由大到小的顺序为。
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2·L-2,沉淀乙的Ksp=1.1×10-10 mol2·L-2。将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙。写出该转化反应的离子方程式:。
(10分)硫酸是工业生产中最为重要的产品之一,也是化学工业的重要原料。
(1)在硫酸工业生产中,我国采用黄铁矿为原料(与氧气反应)生产SO2,进料前必须将黄铁矿粉碎,目的是________。
(2)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择最合适的生产条件是。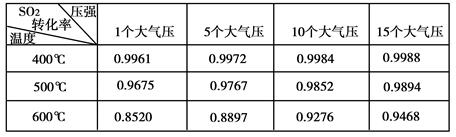
(3)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
已知在T2温度时:2SO2(g)+O2(g)  2SO3(g);△H=-196.6kJ·mol-1,
2SO3(g);△H=-196.6kJ·mol-1,
①在T1温度时,该反应的平衡常数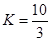 ,若在此温度下,向10L的恒容密闭容器中,充入0.3 mol SO2(g)、1.6mol O2(g) 和0.3 mol SO3(g),则反应开始时正反应速率逆反应速率(填“<”、“>”或“=”)。
,若在此温度下,向10L的恒容密闭容器中,充入0.3 mol SO2(g)、1.6mol O2(g) 和0.3 mol SO3(g),则反应开始时正反应速率逆反应速率(填“<”、“>”或“=”)。
②在T2温度时,开始在10L的密闭容器中加入4. 0 mol SO2(g)和10mol O2(g),一定条件下当反应达到平衡时共放出热量196.6kJ。此时二氧化硫的转化率为。
③在②中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原减小的是(填字母)。
| A.保持温度和容器体积不变,充入1mol O2(g) |
| B.保持温度和容器体积不变,充入2mol SO3 (g) |
| C.降低温度 |
| D.在其他条件不变时,减小容器的容积 |
研究能量的转换,最大限度的提高能量的利用率是化学研究的重要任务之一。
(1)如图为某太空站的能量转化示意图,其中燃料电池用NaOH溶液为电解液。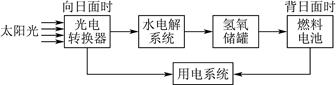
①光电转换器的能量转换形式为。
②水电解系统中通常加入少量Na2SO4,加入Na2SO4的目的是。
③燃料电池的负极反应为:。
(2)以氢氧燃料电池(电极均为石墨电极)为电,用下图装置电解稀硫酸溶液。电解初期d电极附近有大量气泡产生。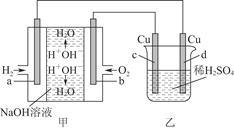
①d电极的名称是。(填“阴极”或“阳极”)
②c电极的电极反应式为:。
③通电初期乙中的总反应为:。
下图为实验室某浓盐酸试剂瓶上的标签,
试根据有关数据回答下列问题:
(1)该浓盐酸的物质的量浓度为_____mol·L—1。
(2)取用任意体积该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。
| A.溶液中Cl-的数目 | B.溶液的密度 | C.溶质的物质的量 | D.溶液的浓度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制450 mL物质的量浓度为0.4 mol/L的稀盐酸,该学生需要量取______mL上述浓盐酸进行配制(结果保留小数点后一位)。若用量筒量取浓盐酸时俯视观察凹液面,则所配制的稀盐酸物质的量浓度将(填“偏高”、“偏低”或“无影响”,下同);若定容摇匀后发现液面低于刻度线,又补加水至刻度线,则所配制的稀盐酸物质的量浓度将。
(4)取100mL 0.4 mol·L—1的盐酸与100mL 0.1 mol·L—1的AgNO3溶液混合,混合后的体积可近似为两溶液的体积之和,则所得溶液中Cl-的物质的量浓度为__ _ __。
现有下列十种物质:
①H2②Cu③Na2O④CO2⑤H2SO4
⑥Ba(OH)2⑦红褐色的氢氧化铁胶体⑧碘酒⑨稀硝酸⑩Al2(SO4)3
(1)按物质的分类方法填写表格的空白处(填写序号):
| 分类标准 |
混合物 |
氧化物 |
电解质 |
| 属于该类的物质 |
(2)⑩在水中的电离方程式为。
(3)写出下列物质之间反应的离子方程式:
少量的④通入⑥的水溶液。
⑤的水溶液与⑥的水溶液混合。
(4)质量都是10 g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是;密度最小的是__ ____。(填分子式)
(5)②与⑨发生反应的化学方程式为:3Cu + 8HNO3 (稀) = 3Cu(NO3)2 + 2NO↑ + 4H2O,__ __ __是氧化剂,__ __ __元素被氧化,参加反应的HNO3中,n(HNO3)被还原∶n(HNO3)未被还原=,当有6.4gCu发生反应时,转移电子的物质的量为mol。