某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
据此判断:
(1)固体B所含物质的化学式为 ;
(2)固体E所含物质的化学式为 ;
(3)反应①的离子方程式为 。
哈佛大学教授Elias James Corey因提出“逆合成分析原理”,将有机合成路线设计技巧艺术的变成了严格的思维逻辑科学而获得1990年诺贝尔化学奖。逆合成分析法可示意如下:
下图是某同学运用逆合成分析法分析合成二乙酸-1,4-环己二醇酯的中间体和基础原料的示意图,请回答有关问题: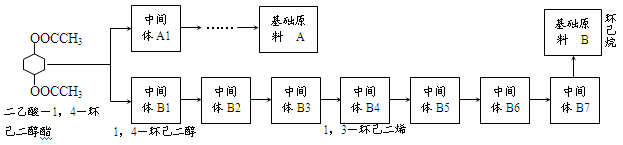
(1)基础原料A的电子式为。由A到A1,最少经过步反应。
(2)写出下列物质转化时的反应条件和反应类型:
①B→B7。反应条件:,反应类型;
②B7→B6。反应条件:,反应类型。
(3)写出下列反应的化学方程式,注明反应条件:
①B5→B4:;
②B3→B2:。
实验室配制少量银氨溶液的方法是先向洁净的试管中加入溶液,然后逐滴加入生成白色沉淀,反应的离子方程式是①______________________________ ;继续滴加至沉淀恰好溶解,即得银氨溶液,反应的离子方程式为②_________________________________;
( 共3分)把2g甲醛气体溶于6g冰醋酸中,再加入4g葡萄糖得混合物甲;另取5g甲酸甲酯和8g乳酸[CH3CH(OH)COOH]混合,得混合物乙;然后将甲和乙两种溶液按7∶4的质量比混合得丙。则甲中碳元素的质量分数为,乙中氢元素的质量分数为,取60g丙完全燃烧,消耗O2的物质的量为 mol。
(7分)在下列物质中选择相应的序号填空:
①甲烷 ②乙烯 ③乙炔 ④甲苯 ⑤1-丁醇 ⑥乙酸乙酯 ⑦甘氨酸
Ⅰ.分子结构为正四面体的是;
Ⅱ.分子中中心原子采取sp杂化的是;
Ⅲ.能发生水解反应的是;
Ⅳ.能与溴水反应并使其褪色的是;
Ⅴ.分子与分子之间存在氢键的是;
Ⅵ.能发生消去反应的是
Ⅶ.与酸或碱都能反应生成盐的是。
(8分)下图装置中,A是由导热材料制成的密闭容器,B是耐化学腐蚀且易于传热的透明气球,关闭K2,将等量1mol的NO2通过K1、K3分别充A、B中,反应起始时,A、B的体积相同均为a L。已知:2NO2(g) 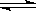 N2O4(g)
N2O4(g) 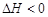
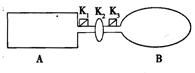
(1)B中可通过判断可逆反应2NO2(g) 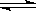 N2O4(g)已经达到平衡。
N2O4(g)已经达到平衡。
(2)若平衡后向A中再充入0.5 mol N2O4,则重新到达平衡后,平衡混合气中NO2的体积分数(填“变小”、“变大”或“不变”)。
(3)若A中到达平衡所需时间为t s,达到平衡后容器内压强为起始压强的0.8倍,则平均反应速率v(NO2)=。
(4)若打开K2,平衡后B的体积缩至0.4a L,则打开K2前,B的体积为。