下列物质中:
(1)互为同分异构体的有 (2)互为同素异形体的有
(3)属于同位素的有 (4)属于同一种物质的有 。(填序号)
①氯;②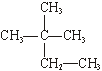 ;③白磷;④氯气;
;③白磷;④氯气;
⑤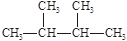 ;⑥
;⑥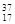 Cl;⑦
Cl;⑦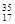 Cl;⑧红磷
Cl;⑧红磷
工业制氢气的一个重要反应是:CO(s)+ H2O(g) ="=" CO2(g) + H2(g)
已知25℃时:C(石墨) +O2 (g) ==CO2(g)△H1 =-394 kJ·mol-1
C(石墨) +1/2O2 (g) ==CO (g)△H2 =-111 kJ·mol-1
H2(g) +1/2O2 (g)==H2O(g)△H3=-242kJ·mol-1
试计算25℃时CO(s)+ H2O(g) ="=" CO2(g) + H2(g)的反应热_______ kJ·mol-1
写出298K时,下列反应的热化学方程式
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量;
(2)N2和O2化合生成184 g NO2气体,吸收热量135.4 kJ;
某河道两旁有甲、乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
(1)甲厂的废水明显呈碱性,故甲厂废水所含的三种离子是______、_______、_______。
(2)乙厂的废水中含有另外三种离子。如果加一定量________(选填:活性炭、硫酸亚铁、硫酸亚铁、铁粉),可能回收其中的金属__________(填元素符号)
(3)另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的__________(填入离子符号)转化为沉淀。经过滤后的废水主要含_____________,可用来浇灌农田。
淀粉的化学式是:;油脂在体内水解后的产物是:
体内缺乏易造成甲状腺肿大的元素是易患龋齿的元素的是。
氯系消毒剂的作用原理:__________________________
明矾净水原理(方程式)_____________________________
漂白粉失效原理(方程式): ___________________________