下图中的均为有机物

据上图回答问题:
(1)的化学名称是
(2)反应③的化学方程式是:
(3)的分子式是:
的结构简式是
(4)符合下列3个条件的的同分异构体的数目有
ⅰ)含有邻二取代苯环结构、 ⅱ)与有相同官能团、ⅲ)不与溶液发生显色反应。
写出其中任意一个同分异构体的结构简式
(5)是的工业原料,用化学方程式表示的一种的工业用途
通常羟基与烯键碳原子相连时,发生下列转化: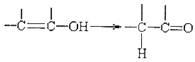
已知有机物A是由C、H、O三种元素组成。原子个数比为2:3:1,其蒸气密度为相同状况下H2密度的43倍,E能与NaOH溶液反应,F转化为G时,产物只有一种结构,且G能使溴水褪色。现有下图所示的转化关系: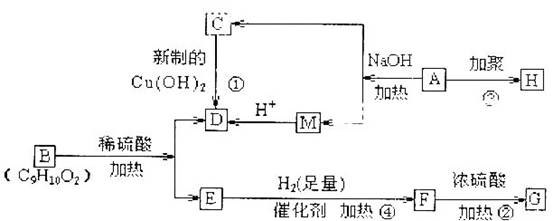
回答下列问题:
(1)写出下列所属反应的基本类型:①,④。
(2)写出B、C的结构简式:B,C。
(3)写出下列化学方程式:反应②。
反应③。
(4)写出所有符合下列条件的B物质的同分异构体
a.含有苯环 b.苯环上只含有一个支链 c.可与NaHCO3溶液反应放出CO2
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属,K是一种红棕色气体,D的俗名叫铁红, A是形成酸雨的主要气体。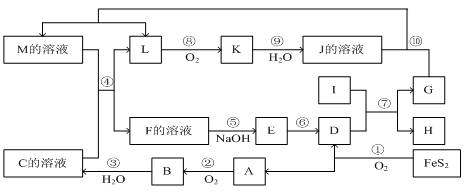
请填写下列空白:
(1)推导出下列物质的化学式:
C:E:
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_________(填写序号)。
(3)在反应⑨中氧化剂与还原剂的物质的量之比为___________________。
(4)反应⑦的化学方程式是:
(5)反应④的离子方程式是:_______________________________________
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其它元素既不在同一周期也不在同主族,B、C、 D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。根据以上信息,回答下列问题:
(1)A和D的氢化物中,沸点较低的是_____________(选填“A”或“D”);A和B的离子中,半径较小的是_______________(填离子符号)。
(2)元素C在元素周期表中的位置_______周期_________族。
(3)已知:晶体的最小重复单位称为“晶胞”。A和E可形成离子化合物,其晶胞结构如图,阳离子(用“●”表示)位于该正方体的顶点或面心;阴离子(用“○”表示)均位于小正方体中。该化合物的电子式__________________。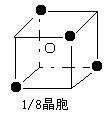
(4)写出B、C两元素各自对应的最高价氧化物的水化物相互反应的离子方程式。
(13分) 如图所示,各物质间有下列转化关系: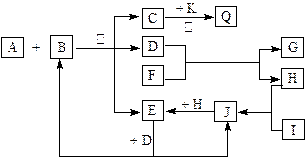
A、F分别为淡黄色固体,A与B的浓溶液反应可以生成C、D、E三种物质,D为无色液体,K为红色金属单质,能在加热条件下与C的浓溶液反应,生成气体Q。I和H为气态双原子分子。反应过程中部分条件和产物均略去。
(1)I的电子式:____________________。
(2)反应A + B的化学方程式:_________________________________________________。
(3)将Q和E按2∶1同时通入品红溶液中,若产物之一含I,则现象可能为___________,原理是(用化学方程式表示)______________________________________________。
(4)若标准状况下将11.2 L Q通入到500 mL 1.5 mol /L 的G溶液中,请将最终溶液的溶质成分及物质的量填入下表(可不填满)。
| 溶质(化学式) |
物质的量 |
(9分) A、B、C、D是中学化学中常见的四种短周期元素。已知①A具有多种同素异形体,A元素原子最外层电子数是次外层电子数的2倍。②B元素最高正价为 + 5。③C元素有多种化合价,且常温下C元素的单质与某种一元碱溶液反应,可得到两种含C元素的化合物。④B、C两种元素质子数之和是A元素质子数的4倍。⑤D是地壳中含量第二的元素,它的单质是一种良好的半导体材料。
(1)写出A元素的名称_________和C离子的结构示意图____________。
(2)工业上利用A的单质来制备单质D,请写出相应的方程式:
________________________________________________________________________。
(3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种见的漂白性物质和一种能使石蕊试纸变蓝的气体。则X的分子式。X分子中B、C原子间的化学键的类型为___________(填“极性键”或“非极性键”)。X与水反应的化学方程式________________________。