下图(左)是还原铁粉与水蒸气反应的实验装置,实验时,B中灰色的铁粉变为黑色,且生成的黑色固体物质是一种可溶于稀盐酸的较复杂化合物。请回答下列问题: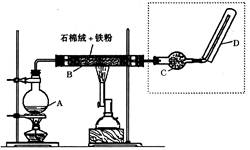
(1)B中发生反应的化学方程式为 。
(2)反应前A中投放碎瓷片的目的是 。
(3)某次实验后,取B中的固体物质少量,溶于足量稀盐酸,再滴加KSCN溶液。
溶液颜色无明显变化,试解释原因 。
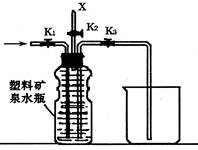
(4)上图(左)中虚线部分,可以用右图所示装置代替,在X口点燃收集到的气体即可检验H2的存在。实验开始时,打开K1.K2,关闭K3,使反应先进行一段时间之后,必须进行 操作,方可关闭K2.打开K3,再收集气体。当收集到半瓶气体时,停止加热,关闭K1,若要使H2顺利逸出而进行点燃实验,操作的方法是 。
(5)替代装置未像原装置那样使用干燥管,同样顺利完成了实验,原因是 。
在题后横线上简要说明不正确使用化学仪器可能造成的不良后果。
(1)把容器放在桌上使劲塞进塞子:______________________________________________。
(2)加热盛有碱式碳酸铜的试管,试管外壁有水:__________________________________。
(3)将加热后的蒸发皿直接放在实验台上:________________________________________。
(4)加热液体时,试管口朝着有人的方向:________________________________________。
实验室要配制2.0 mol·L-1 KNO3溶液100 mL,不使用的化学仪器是()
①烧杯②250 mL容量瓶③100 mL容量瓶④玻璃棒⑤胶头滴管⑥托盘天平
| A.只有② | B.②⑥ | C.①③ | D.①④ |
普利斯特里(Joseph Priestley)在拉瓦锡之前发现了氧气,但由于受“燃素说”的影响,他把氧气当作了“燃素”。拉瓦锡正是在普利斯特里研究的基础上,破除了“燃素说”的束缚,确认氧气是由一种元素形成的纯净物。普利斯特里在一次加热浓硫酸的实验中,由于不慎,造成了倒吸,将水槽中的水银(Hg)倒吸进加热后的浓硫酸中,并且烧坏了手。偶然中他发现热的浓H2SO4与水银发生了反应并生成了一种气体。这种气体就是由他发现的SO2。根据以上叙述判断下列说法不正确的是()
| A.浓H2SO4具有强腐蚀性,操作应格外小心 |
| B.为防止倒吸,实验结束时应先从水槽中取出导气管,后撤酒精灯 |
| C.实验中应仔细观察,不放过任何异常现象 |
| D.普利斯特里是一位失败的科学家,不值得尊敬 |
某同学在实验室发现两瓶白色固体,一瓶是硫酸钠,另一瓶是碳酸钠,但均已失去标签。下面是该同学检验这两瓶固体的方法,其中不能成功检验出硫酸钠和碳酸钠的是()
| A.分别取固体少许加入试管中,配成溶液,然后滴加氯化钡溶液 |
| B.分别取固体少许加入试管中,配成溶液,然后滴加氯化钡溶液,最后滴加盐酸 |
| C.分别取固体少许加入试管中,配成溶液,然后滴加盐酸,最后滴加氯化钡溶液 |
| D.分别取固体少许加入试管中,配成溶液,然后滴加盐酸酸化的氯化钡溶液 |
2006年6月1日讯中共中央政治局常委、国务院总理温家宝近日就2006年环保专项行动作出重要批示,部署2006年整治违法排污企业保障群众健康环保专项行动。水、大气、土壤等污染日益严重,重金属、有毒化学物质和持久性有机物等污染持续增加。一些地方已经喝不到干净的水,呼吸不到清洁的空气,土壤污染严重危及农产品安全。环境污染和生态破坏造成了巨大经济损失,严重危害群众健康,成为人民群众的切肤之痛。环境污染问题是举世瞩目的社会热点问题,下列收集气体的方法既能达到收集目的又符合环保要求的是()
A.用如图所示的方法收集二氧化硫(二氧化硫的密度比空气大)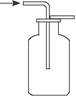 |
B.用下图所示的方法收集二氧化氮(已知:二氧化氮的密度比空气的密度大、有毒但能溶于氢氧化钠溶液)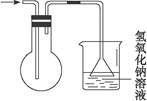 |
C.用右图所示的方法收集一氧化碳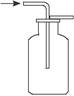 |
D.用右图所示的方法收集氢气 |