原电池是把 转化成 的装置,其反应的实质是 。在铜锌原电池(稀硫酸为介质)中:
正极材料是 ,其电极反应式: ;
负极材料是 ,其电极反应式: ;
胡萝卜中含有大量的β-胡萝卜素,被人体吸收后可转化成视黄醇(即维生素A),是目前最安全补充维生素A的产品。在体内酶的催化下,1 mol β-胡萝卜素可氧化为2 mol视黄醛,然后再转化为视黄醇,其过程如下:
已知:
完成下列填空:
(1)β-胡萝卜素的化学式为_________________。反应I的类型为_________。
(2)β-胡萝卜素在人体吸收时需要相应的溶剂,下列适合作为溶剂的是________(选填编号);
a. 水 b. 油脂 c. 苯 d. 乙醇
许多保健品中都含有β-胡萝卜素,从其结构推测可能的作用是________(选填编号)。
a. 提供蛋白质 b. 补充微量元素 c. 抗氧化剂 d. 调节pH
(3)视黄醛的一种同分异构体属于萘( ,C10H8)的衍生物,其可能具有的化学性质有________(选填编号)。
,C10H8)的衍生物,其可能具有的化学性质有________(选填编号)。
a. 与溴水发生加成反应 b. 能与氯化铁溶液发生显色反应
c. 发生银镜反应d. 能使酸性高锰酸钾溶液褪色
(4)丁烯酮(CH2=CHCOCH3)是合成视黄醇和β-胡萝卜素的重要原料之一。工业上采用如下流程合成丁烯酮: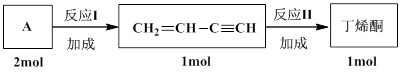
写出A的结构简式:__________。写出反应II的化学方程式:___________________。
1200℃时可用反应 2BBr3(g)+ 3H2(g)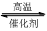 2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空:
2B(s) + 6HBr(g) 来制取晶体硼。完成下列填空:
(1)下列说法能说明该反应达到平衡的是______(选填序号,下同)。
a. v正(BBr3)= 3v逆(HBr) b. 2c(H2) = c(HBr)
c.密闭容器内压强不再变化 d. 容器内气体平均摩尔质量不再变化
(2)若密闭容器体积不变,升高温度,晶体硼的质量增加,下列说法正确的是_________。
a. 在平衡移动时正反应速率先增大后减小
b. 在平衡移动时逆反应速率始终增大
c. 正反应为放热反应
d. 达到新平衡后反应物不再转化为生成物
(3)若上述反应在10L的密闭容器内反应,5min后,气体总质量减少1.1 g,则该时间段内氢气的平均反应速率为__________________。
(4)往容器中充入0.2 mol BBr3和一定量H2,充分反应达到平衡后,混合气体中HBr百分含量与起始通入H2的物质的量有如图关系。在a、b、c三点中,H2 的转化率最高的是______(选填字母)。b点达到平衡后,再充入H2使平衡到达c点,此过程中平衡移动的方向为__________(填“正向”、“逆向”或“不移动”)。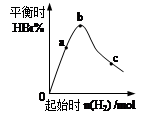
下表中所列的字母分别代表某一化学元素。完成下列填空:
| a |
|||||||||||||||||
| b |
|||||||||||||||||
| c |
d |
e |
f |
||||||||||||||
| g |
|||||||||||||||||
| h |
|||||||||||||||||
| i |
|||||||||||||||||
(1)h的最外层有____种运动状态的电子。a、b、c三种元素形成的化合物电子式为________。
(2)d单质溶于i的最高价氧化物对应水化物的溶液时发生反应的离子方程式为____________。
(3) 元素e与f元素相比,非金属性较强的是__________(写元素符号),下列表述中能证明这一事实的是__________(选填序号)。
a. e的阴离子还原性强于f的阴离子 b. f的氢化物酸性强于e的氢化物
c. e单质的熔点高于f单质 d. e和f形成的化合物中,e显正价,f显负价
(4)元素X(非a~i元素)是所在周期原子半径最大的非金属元素,它的气态氢化物为三角锥形极性分子,写出X在周期表中的位置_______________________________。
某化合物A经碱性水解后得到B,酸化后得到C(C8H8O2)。核磁共振氢谱表明,C含有苯环,且苯环上有2种氢原子。B经过下列各步反应后得到G(C8H12O4),核磁共振氢谱显示G中只有1种氢原子。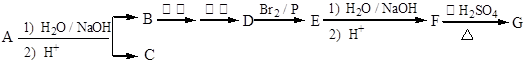
已知: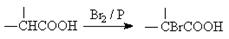
请回答下列问题:
(1)有机物类别:A物质属于______类,C物质属于________类。
(2)写出满足下列条件的C的所有同分异构体:__________________________________________。
①是苯的对位二取代化合物;②能与FeCl3溶液发生显色反应;③不考虑烯醇( )结构。
)结构。
(3)写出F→G反应的化学方程式:_____________________________________________________。
(4)写出A的结构简式:_____________________________________。
(5)在G的粗产物中,经检测含有聚合物杂质。写出聚合物杂质可能的结构简式(仅要求写出1种):__________________________________。
F是新型降压药替米沙坦的中间体,可由下列路线合成:

(1)D→E的反应类型是_________,E→F的反应类型是__________________________。
(2) C中含有的官能团名称是_________。已知固体C在加热条件下可溶于甲醇,下列有关C→D的说法正确的是____________________。
a.使用过量的甲醇,是为了提高D的产量 b.浓硫酸的吸水性可能会导致溶液变黑
c.甲醇既是反应物,又是溶剂 d.D的化学式为C9H9NO4
(3)E的同分异构体苯丙氨酸(a-氨基-ß-苯基丙酸)经缩合反应形成的高聚物是________(写结构简式)。