第4周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7。其原子序数按A、B、C、D顺序增大,已知A与B的次外层电子数为8,而C与D次外层电子数为18,根据结构填空:
(1)写出元素名称:A ,B ,C ,D 。
(2)D的简单离子是 。
(3)元素的氢氧化物碱性最强的是 。
(4)B与D二原子间能形成化合物的化学式是 。
(5)写出A、B的电离能顺序 。
(6)写出C基态原子的电子排布式 。
某学生做浓硫酸性质的实验:在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃管口处缠放一团蘸有NaOH溶液的棉花。加热试管,观察现象。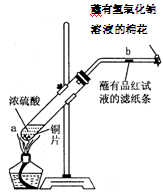
回答下列问题:
(1)写出试管中发生反应的化学方程式。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为,待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为。
(3)蘸有NaOH溶液的棉花团作用是。
(4)硫酸型酸雨的形成过程可用下列反应中的来表示。
A:SO2+H2O H2SO3
H2SO3
B:O2+2H2SO3=2H2SO4
C:SO2+H2O2=H2SO4
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,其中物质E是气体丙的水溶液,物质H是红褐色沉淀。它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。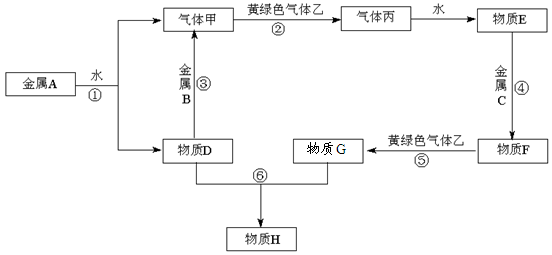
请根据以上信息回答下列问题:
(1)写出A、C、丙的化学式:
A、 C、丙
(2)写出反应③的化学方程式:,
反应⑤的离子方程式:。
已知某待测液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干种离子组成,进行如下实验:第一步:加入过量的稀盐酸,有白色沉淀生成。
第二步:过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
第三步:再过滤,取少量滤液,滴入NaOH溶液至溶液呈碱性,在此过程中溶液无明显现象,加热该溶液,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:
(1)分别写出第二步和第三步中所涉及的反应的离子方程式:
第二步:第三步:;
(2)待测液中一定含有、NO3-离子,一定不含有离子,还有一种离子不能确定其是否存在,要检验这种离子的实验方法是(填写实验名称和观察到的现象及结论,不要求写实验操作过程),。
(1)在一个白色点滴板的二个孔穴中分别加入火柴梗、少量CuSO4·5H2O。分别滴入几滴浓硫酸,观察现象。回答下列问题:
浓硫酸滴到火柴梗上,火柴梗变________(填实验现象),说明浓硫酸具有________性。
浓硫酸滴入CuSO4·5H2O中,胆矾(填实验现象),说明浓硫酸具有_________性。
(2)为探究Fe3+能转化为Fe2+,实验室提供下列试剂:铁粉、0.1mol·L-1 FeCl3溶液、0.1mol·L-1 FeCl2溶液、KSCN溶液、新制氯水。请你就实验操作、实验现象、结论完成以下填空:
取少量溶液于试管中,加入足量,充分振荡后静置,滴加1至2滴,无明显变化,说明Fe3+已转化为Fe2+。
以下是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空: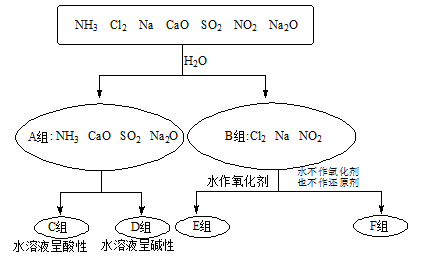
(1)上述第一级分类标准(分成A、B组的依据)是。
(2)F组中物质除了Cl2外还有(填化学式)
(3)D组中的氨水呈弱碱性,用电离方程式表示呈弱碱性的原因:。
(4)由Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,说明理由:。