控制适合的条件,将反应 设计成如右图所示的原电池。下列判断不正确的是
设计成如右图所示的原电池。下列判断不正确的是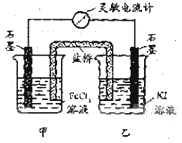
| A.反应开始时,乙中石墨电极上发生氧化反应 |
| B.反应开始时,甲中石墨电极上Fe3+被还原 |
| C.电流计读数为零时,反应达到化学平衡状态 |
| D.电流计读数为零后,在甲中溶入FeCl2固定,乙中石墨电极为负极 |
下列说法不符合生产实际的是( )
| A.硫酸生产中,SO2催化氧化选择1~10 MPa、400~500 ℃条件下进行 |
| B.尾气中含有少量SO2,可用石灰水吸收,然后再用硫酸处理 |
| C.工业上,常采用以铁为主的催化剂,在400~500 ℃和10~30 MPa的条件下合成氨 |
| D.造气中产生的CO,可在催化剂作用下,与水蒸气反应生成CO2和H2 |
下列各个装置中铁棒被腐蚀由易到难的顺序是正确的是()
① ② ③ ④
| A.③①②④ | B.④①③② | C.①③②④ | D.②④①③ |
已知:CaCO3(s)===CaO(s)+CO2 (g) ΔH>0,ΔS>0.则该反应能自发进行的条件是( )
| A.低温 |
| B.高温 |
| C.任何温度下都能自发进行 |
| D.任何温度下都不能自发进行 |
下列说法不正确的是( )
| A.自发反应在恰当条件下才能实现 |
| B.所有的化学反应都有能量变化 |
| C.升高温度,活化分子百分数增大,化学反应速率一定增大 |
| D.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
家用炒菜铁锅用水清洗放置后,常出现红棕色的锈斑,在此变化过程中不发生的化学反应是()
| A.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | B.Fe-3e-=Fe3+ |
| C.2Fe+2H2O+O2=2Fe(OH)2↓ | D.2H2O+O2+4e=4OH- |