某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8~9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题
(1)上述实验中的过滤操作需要玻璃棒、______________、______________等玻璃仪器。
(2)步骤1过滤的目的是__________________________________________。
(3)当步骤2中的溶液pH=8~9时,检验沉淀是否完全的方法是____________。
实验是化学研究的一种重要手段,现有下图所示A~G七种仪器,请根据要求填空。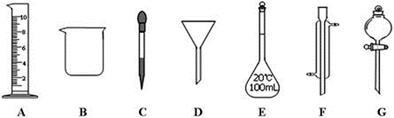
(1)写出仪器名称:E ,F
(2)下列实验操作中用到仪器G的是 (选填下列选项的编号字母)。
a.分离水和CC14的混合物
b.分离水和酒精的混合物
c.分离水和泥砂的混合物
(3)实验室配制100mL 0.5mol/L的盐酸溶液。
①下列关于仪器E的使用方法中,正确的是 (选填下列选项的编号字母)。
a.使用前应检查是否漏液b.使用前必须烘干
c.不能用作物质反应或溶解的容器 d.热溶液可直接转移到容量瓶中
②需要10mol/L的浓盐酸 mL。取用该体积盐酸时,需要用到上述仪器中的A和 (选填仪器的编号字母)。
刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式:Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
(1)请在上式中标出电子转移的方向和数目
(2)该反应的氧化剂是
(3)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是 (填序号)
| A.氯气 | B.铁 | C.铜 | D.稀硫酸 |
化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为 ,其能消毒杀菌是因有强 性。
(2)KAl(SO4)2•12H2O的俗名为 ,因其溶于水生成 而具有净水作用。
(3)酸雨的pH小于 ,含亚硫酸的酸雨久置后pH (增大、减小或不变)。
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为 。
下图所示装置可用于多种实验。
(1)实验室可利用该装置来制取氯气,发生反应的化学方程式为:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
①用双线桥标出上述反应中的电子转移情况。
②B装置的作用是___________________,C装置中盛装的液体最好是 。
③若按上述反应制得的氯气体积为4.48 L(标准状况),则实际反应中消耗12 mol/L盐酸的体积大于理论值__________mL。
(2)在实验室要测定部分变质的过氧化钠的纯度,也可用上图装置中的部分仪器。
①上述装置中多余的仪器是_____________(填A、B、C、D等序号)。 ②要完成上述实验目的,圆底烧瓶中发生反应的化学方程式为____________________。
②要完成上述实验目的,圆底烧瓶中发生反应的化学方程式为____________________。
③若取用样品的质量为2.5 g,收集到气体的体积为280 mL(标准状况),则样品中Na2O2的纯度为___________。
有10mL NaOH溶液,向其中通入一定量的CO2,得到了Na2CO3和NaHCO3的混合溶液。向所得溶液中逐滴加入0.1mol/L的盐酸,边加边振荡,使其充分反应,产生CO2气体的体积(标准状况)与所加盐酸体积之间的关系如下图所示。
请回答下列问题:
(1)向Na2CO3和NaHCO3的混合溶液中滴加盐酸时发生反应的离子方程式为
, ;
(2)混合溶液中Na2CO3和NaHCO3的物质的量之比为 ;
(3)原NaOH溶液中NaOH的物质的量浓度为 ,所通CO2气体的体积在标准状况下为 。