A、B、C、D、E均为可溶于水的固体,组成它们的离子有分别取它们的水溶液进行实验,结果如下: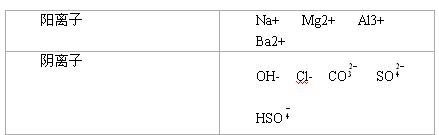
①A溶液与B溶液反应生成白色沉淀和气体,且沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀溶于E溶液且产生气体;
③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;
④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
(1)据此推断它们是:
A ;B ;C ;D ;E 。
(2)B溶液与过量D溶液反应的离子反应方程式________________ _
_________________________
A、B、C、D、E是相邻三个周期中的五种元素,它们的原子序数依次增大,B、C、D属同一周期,A、E在周期表中处于同一纵行。已知:
①除A外,各元素原子的内层均已填满电子,其中B的最外层有4个电子;
②A与B,B与C都能生成气态非极性分子的化合物;
③D与E生成离子化合物,其离子的电子层结构相同。
回答:
(1)A为________元素,B为________元素,C为________元素,D为________元素。
(2)C元素在周期表中属________周期________族元素,其原子电子排布式为________。
(3)B与C形成的非极性分子的电子式是________。其中共价键类型及数目是________。(填σ键或π键)
如图所示为高温超导领域里的一种化合物——钙钛矿晶体结构,该结构是具有代表性的最小重复单位。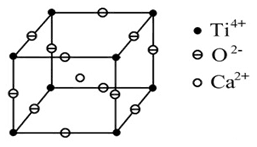
(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的氧离子、钙离子各有 、 个。
(2)该晶体结构中,元素氧、钛、钙的离子个数比是 ,该物质的化学式可为 。
(3)若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构图中正方体边长(钛原子之间的距离)为d nm(1 nm=10-9 m),阿伏加德罗常数为6.02×1023 mol-1,则该晶体的密度为 g·cm-3。
石墨的片层结构如图所示,试完成下列各题:
(1)平均 个碳原子构成一个正六边形。
(2)石墨晶体每一层内碳原子数与C—C化学键之比是 。
某有机物的结构式如下: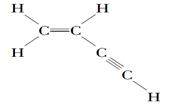
则分子中有________个σ键,________个π键。
(1)CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是________(填“极性”或“非极性”)分子。
(2)在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的空间构型是________。CO2与CS2相比,________的熔点较高。