按题给信息完成方程式(注意:有机物要写结构简式)
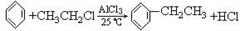
(1)R—Br+2Na+Rˊ—Br —→ Rˊ—R+2NaBr,Rˊ、R为烃基,可相同,也可不相同。
则CH3CH2Br+CH2=CHBr+2Na—→_______ ________。
(2)傅瑞德尔-克拉福茨反应是在苯环上引入烷基的反应,例如:
|
按要求填写下列相关内容:
(1)在常温下,将体积为VaL、pH为a的稀硫酸和体积为VbL、pH为b的烧碱溶液混合,若所得混合液为中性。如果a+b=15,则Va:Vb=___________。某温度时,水的离子积常数Kw=1×10-13.在此温度下,将pH=a的硫酸溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,如果a+b=12,则Va:Vb=___________。
(2)中和相同体积,相同pH的Ba(OH)2、NH3·H2O、NaOH三种稀溶液所用相同浓度的盐酸的体积分别为V1、V2、V3,则三种关系为______________(用“V1、V2、V3”和“>、<、=”表示)。
(3)今有A.盐酸 B.醋酸 C.硫酸三种酸。
①在同体积、同pH的三种酸中,分别加入足量的碳酸氢钠粉末,在相同条件下产生CO2的体积由大到小的顺序是___________。(填酸的序号并用符号“>、<、=”连接,下同)
②在同体积、同pH的三种酸中,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的氢气(同温同压下),则开始反应时速率大小关系是__________,反应所用时间长短关系是_____________。
金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质。
(1)钠与水反应时,钠漂浮在水面上。甲同学用刺有小孔的铝箔将4.6g的钠包裹,而后投入到水中,使钠沉入水底与水(足量)反应。该过程中发生反应的离子方程式有___________,充分反应生成的气体体积_________(填“大于”、“小于”或“等于”)2.24L(标准状况下)。
(2)乙同学将足量的铜粉投入到500mL18.4mol/L的浓硫酸中并加热制取SO2,写出该反应的化学方程式__________,生成的SO2物质的量小于4.6mol的原因是_____________。
(3)丙同学向MgCl2、AlCl3的混合溶液中逐滴滴加2mol/L的NaOH溶液,并绘制出沉淀与NaOH溶液体积的关系图像如图,则a=_________,b=________。
无机化合物可根据其组成和性质进行分类:
(1)下图所示的物质分类方法名称是________________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
①HCl ②_______ |
③_______ ④Ba(OH)2 |
⑤Na2CO3 ⑥________ |
⑦CO2 ⑧Na2O2 |
(3)写出⑦转化成⑤的化学方程式________________________。
(4)呼吸面具中用⑧作为O2来源的反应原理为:______________________。
(5)实验室制备⑦常用_______和_________反应,检验该气体的方法是______________________。
一定温度下,在容积固定的VL密闭容器中加入nmolA、2nmolB,发生反应:A(g)+2B(g)  2C(g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) △H<0,反应达到平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡,则下列说法中正确的是_______________(填字母)。
A.物质A、B的转化率之比为1:2
B.起始时刻和达到平衡后容器中的压强之比为3n:(3n-nx)
C.充入惰性气体(如Ar),平衡向正反应方向移动
D.当2v正(A)=v逆(B)时,反应一定达到平衡状态
(2)K和x的关系满足K=__________(用含V、n、x的表达式表示)。
(3)该反应的逆反应速率与时间的关系如图所示:
①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都仅改变了一种条件,试判断改变的条件:
t2时____________;t8时____________。
②t2时平衡向_________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率随时间变化的曲线。
电化学原理在能量转换、物质合成、防止金属腐蚀等方面应用广泛。
I.下列是常见的电化学示意图
(1)图①是碱性锌锰电池的构造示意图,在正极反应的物质是_______________(填“Zn”或“MnO2”),正极发生_______反应(填“氧化”或“还原”)。
(2)图②是酸性电解质的氢氧燃料电池工作原理示意图,B极发生的电极反应是________________。
(3)图③表示钢铁发生吸氧腐蚀生锈的示意图,写出氧气发生的电极反应:___________________。
(4)能表示“牺牲阳极的阴极保护法”的示意图是______________(填序号)。图④中,钢闸门连接电源的_____________极而受到保护。在图⑤中标出电子的移动方向。
II.下列是常见的电化学装置图。
(5)图⑥中电池的总反应为__________________(写化学方程式),盐桥中装有含琼胶的KCl饱和溶液,盐桥中Cl-会向_______________(填“左”或“右”)边烧杯中的溶液移动。
(6)检验图⑦中阳极产物的方法和现象是________________。