(8分)在反应: Fe2O3 +2 Al = Al2O3 + 2Fe 中,______元素的化合价升高,该元素的原子______电子,被________;______元素的化合价降低,该元素的原子______电子,被_________;该反应中,___________是氧化剂,___________是氧化产物。
如图为电解装置,X、Y为电极材料,a为电解质溶液。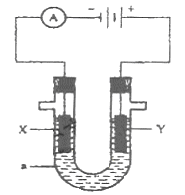
(1)若a为含有酚酞的KCl溶液,X为Fe,Y为石墨,电解一段时间后:
X电极附近可观察到的实验现象是;
写出Y电极的电极反应式。
(2)若要实现Cu +H2SO4=CuSO4+H2↑,
则Y电极材料是;
写出X电极的电极反应式。
(3)若要利用该装置在铁制品表面镀上一层银,则a为 ,反应前两电极的质量相等,反应后电极质量相差2.16g,则该过程理论上通过电流表的电子数为。
(4)若X、Y均为惰性电极,a为NaOH溶液,电解一段时间后,溶液的pH (填“增大”“不变”“减小”),若要使溶液恢复原来的状态,可往溶液中加入 。
请按要求填空:
I.现有:①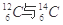 、② O2与O3、③ 正丁烷与异丁烷、④ 金刚石与石墨、⑤ 冰与水、⑥ 乙醇与二甲醚。请用序号填写对应的分类:
、② O2与O3、③ 正丁烷与异丁烷、④ 金刚石与石墨、⑤ 冰与水、⑥ 乙醇与二甲醚。请用序号填写对应的分类:
(1)互为同位素的是( );
(2)互为同素异形体的是();
(3)互为同分异构体的是();
(4)属于同一化合物的是( )
II.现有以下物质:①NaCl晶体 ②液态(纯)H2SO4 ③液态的(纯)醋酸 ④汞(金属) ⑤纯蔗糖(C12H22O11) ⑥酒精(C2H5OH) ⑦熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是(),
(2)以上物质中属于电解质的是(),
(3)以上物质中属于非电解质的是( ),
(4)以上物质中溶于水后形成的水溶液能导电的是( )。
(12分)如图装置闭合电键时,电流计A的指针将发生偏转。试回答下列问题。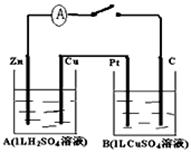
(1)A池是____________;Zn的电极名称是____________;B池是____________;
Pt的电极名称是____________(填电解池、原电池、阴、阳、正、负极等)
(2)写出下列有关反应:C极上电极反应:_________________
(3)B池中的总反应的化学方程式为________________________
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)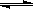 C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。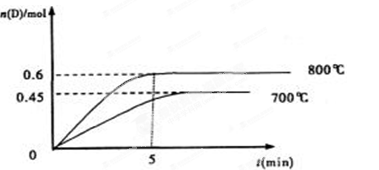
试回答下列问题:
(1)800℃时,0—5min内,以B表示的平均反应速率为________。
(2)能判断该反应达到化学平衡状态的依据是________。
A.容器中压强不变B.混合气体中c(A)不变
C.2v正(B)=v逆(D)D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K=______,该反应为_____反应(填吸热或放热)。
依据氧化还原反应:2Ag+(aq)+Cu(s)===Cu2+(aq)+2Ag(s)设计的原电池,如图所示。请回答下列问题: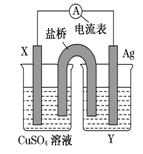
(1)电极X的材料是________;电解质溶液Y是________溶液。(填名称)
(2)银电极为电池的________极,发生的电极反应为____________________________;X电极上发生的电极反应为____________________________。
(3)外电路中的电子是从________极流向______极(填电极材料)。外电路中每通过0.1 mol电子,银电极的质量理论上增加g。
(4)原电池工作时,盐桥(装有琼脂-KCl的U型管)里的Cl-移向电极。