在一个容积固定不变的密闭容器中进行反应:2A(g)+B(g)==3C(g)+D(s),已知将2molA和1molB充入该容器中,反应在某温度下达到平衡时,C的物质的量为Wmol,C在平衡混合气体中的体积分数为n%。
⑴可认定上述可逆反应在一定条件下已达到化学平衡状态的是 (选填序号)。
A、体系压强不再变化 B、v正(A)=2v逆(B)
C、体系的密度不再变化 D、混合气体的平均相对分子质量不再变化
⑵如果用下列情况的配比作起始物,在同样的容器和温度下达到平衡,其结果一定是:
C的物质的量为2Wmol,C在平衡混合气体中的体积分数仍为n%的是
A、4molA+2molB B、6molC+1molD
C、1molA+0.5molB+1.5molC+0.5molD D、2molA+1molB+3molC+1molD
E、2molA+1molB+3molC+2molD
⑶若维持该题条件不变,仅从生成物开始配比,要求达到平衡时,C的物质的量仍为Wmol,则D的起始物质的量n(D)应满足的条件是 (用含W的代数式表示)
⑷此反应的v—t图象如甲图,若其他条件都不变,只是在反应前加入合适的催化剂,则
其v—t图象如乙图,请用“=、<、>”填空:①a1 a2;②b1 b2;③两图中
阴影部分面积:甲 乙。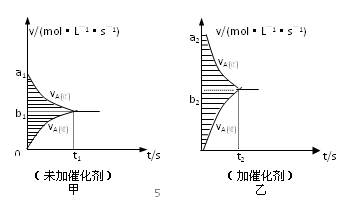
铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:。
(3)将装置C中两种液体分离开的操作名称是。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为。
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,二是。
(3)由MgCl2溶液得到MgCl2·6H2O晶体,操作为、 、
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:。
②由MgCl2·6H2O加热制备无水MgCl2的操作在氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
(1)汽车内燃机工作时会引起N2和O2的反应:N2(g)+ O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。
2NO(g),是导致汽车尾气中含有NO的原因之一。
①在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如图所示,根据图像判断反应N2(g)+ O2(g) 2NO(g)的△H__________0(填“>”或“<”)。
2NO(g)的△H__________0(填“>”或“<”)。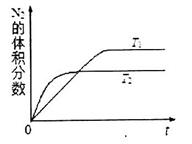
②在T3温度下,向2L密闭容器中充入10molN2与5mo1O2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率v(N2)=___________________。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为____________。
(2)利用下图所示装置(电极均为惰性电极)可吸收SO2,用阴极排出的溶液可吸收NO2。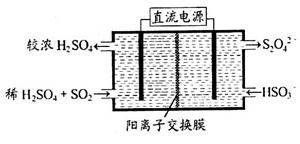
①阳极的电极反应式为_____________________。
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32—生成。该反应中氧化剂与还原剂的物质的量之比为_______________。
(3)以H2O2和硼氢化合物NaBH4(B的化合价为+3价)作原料的燃料电池,可用作电解池的电源。其工作原理如图所示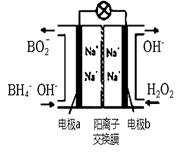
①写出a极上的电极反应式:,
②正极材料采用MnO2,MnO2除了作电极材料之外还可能具有的作用为
某工业废水中含有CN-和Cr2O72—等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理: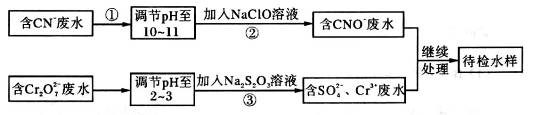
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为________________。
(2)步骤③的反应为S2O32—+ Cr2O72—+H+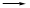 SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
SO42—+Cr3++H2O(未配平),则每消耗0.4mol Cr2O72—转移__________mol e-。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是____________________。
(4)在25℃下,将amol·L—1的NaCN溶液与0.01mol·L-1的盐酸等体积混合,反应后测得溶液pH=7,用含a的代数式表示HCN的电离常数Ka=_________________。若25ºC 时Ka=1×10-9则同体积均为0.1mol·L-1的NaCN、HCN的混合溶液中下列说法不正确的是
a.此溶液一定有C(Na+)+C(H+)=C(OH‾)+C(CN‾)
b.混合溶液中水的电离程度一定大于该温度下纯水的电离程度。
c.此溶液一定有C(Na+)="C(HCN)+" C(CN‾)
d.此溶液加入少量氢氧化钠或盐酸溶液的PH值变化不大
(5)取工业废水水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀。该过程中反应的离子方程是____________。
(10分)短周期中五种元素A、B、C、D、E原子序数依次增大,其中A、B、C原子核外电子层数之和是5,且C原子最外层上的电子数为A和B两元素原子最外电子层上电子数的总和,C原子的价电子构型为nsnnpn+1,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题:
(1)B、C、D、E四种元素的原子,半径从大到小的顺序是
(填元素符号或化学式,下同);第一电离能从大到小的顺序是
(2)由A、C两种元素形成的离子化合物中C元素的质量分数为73.68%,它的所有原子最外层都符合相应的稀有气体原子的最外层电子层结构,该物质加热时就能分解为两种气体,则X的化学式为,X受热分解的化学方程式为_____________________。
(3)C和E形成一种离子化合物Y,其摩尔质量为65 g/mol,Y受热或撞击时立即分解为两种单质。则Y的化学式为,Y的阴离子是一种弱酸根离子,全由C元素组成,与Y的阴离子具有相同原子数和电子数的分子有(任写一种),Y与盐酸反应的离子方程式为。
(4)(CA4)2SO4溶液加水稀释时,溶液中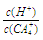 的值将(填“增大”、“减少”或“不变”)。
的值将(填“增大”、“减少”或“不变”)。
(1)一定温度下,向1 L 0.1 mol·L-1 CH3COOH溶液中加入0.1 mol CH3COONa固体,则醋酸的电离平衡向________(填“正”或“逆”)向移动;溶液中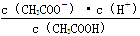 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3 CH3COONa+CO2↑+H2O。
CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,Kw=1.0×10-12,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_____________________________。
②该温度下,将0.01 mol·L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气_____。
| A.盐酸多 | B.H2A多 | C.一样多 | D.无法确定 |
④将0.1 mol·L-1 H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为_______________________________________。