在稀氨水中存在平衡:NH3+H2O NH
NH +OH-,如进行下列操作,则NH3、NH
+OH-,如进行下列操作,则NH3、NH 、H+、OH-浓度及PH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3) ,c(H+) ,PH值 。
、H+、OH-浓度及PH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3) ,c(H+) ,PH值 。
(2加入少量NaOH固体时,c(NH ) ,c(OH-) ,PH值 。
) ,c(OH-) ,PH值 。
(3)加入NH4Cl晶体时,c(NH ) ,c(OH-) 。
) ,c(OH-) 。
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。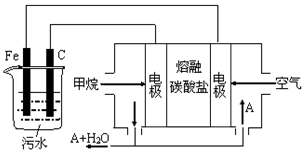
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的__________。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH。
(2)电解池阳极能同时发生了两个电极反应(阳极上还会产生微量气泡),电极反应式分别是:Ⅰ.___________________________;Ⅱ.___________________________________;
(3)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是______________________;
②正极的电极反应是________________________________;
③为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是_________________;
已知某二元酸(化学式用H2RO4表示)在水中的电离方程式为: H2RO4=H++HRO4-;HRO4 H++ RO42-回答下列问题:(1)NaHRO4溶液显(填“酸性”、“中性”或“碱性”),理由是_________
H++ RO42-回答下列问题:(1)NaHRO4溶液显(填“酸性”、“中性”或“碱性”),理由是_________
(用离子方程式和必要的文字说明)。
(2)Na2RO4溶液湿(填“酸性”、“中性”或“碱性”),理由是__________ (用离子方程式表示)
(3)如果25℃时,0.1 mol/L的NaHRO4溶液中,c(RO42-)=0.029 moL/L,则0.1mol/L H2RO4溶液中c(RO42-)0.029 mol/L(填“<”、“>”或“=”),理由是。
(4)25℃时,0.1 mol/L的NaHR04溶液中,各离子浓度由大到小的顺序是。
)氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。(1)上图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式。
(2)已知:N2(g)+ O2(g)=" 2" NO(g)△H = +180 kJ • mol-1
2NO(g)+2 CO(g)= N2(g) + 2 CO2(g)△H =" -" 746 kJ • mol-1
则反应CO(g) + O2(g)= CO2(g)的△H = kJ • mol-1
O2(g)= CO2(g)的△H = kJ • mol-1
(3)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g)△H <0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为,该反应的平衡常数表达式K =。
2NH3(g)△H <0,若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为,该反应的平衡常数表达式K =。
(4) 在固定体积的密闭容器中,1.0×103kPa时反应 N2(g)+3H2(g) 2NH3(g)
2NH3(g)
△H<0 的平衡常数K与温度T的关系如下表:
| T/K |
298 |
398 |
498 |
| 平衡常数K |
51 |
K1 |
K2 |
①K1K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是(填字母)
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.NH3的浓度保持不变
c.容器内压强保持不变 d.混合气体的密度保持不变
(1)将各有机物的序号填到对应分类中①CH3CH2CH3②CH2=CH—CH3 ③CH3COOCH3④H3C—OH⑤CH3CH2COOH醇:_______羧酸:_______ 烷烃: ______
⑥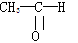 烯烃:_______酯:_______醛:_______
烯烃:_______酯:_______醛:_______
(2)如下图所示的核磁共振谱图是1-丙醇: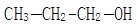 和2-丙醇:
和2-丙醇: 中的一种,根据图中信息,其结构简式为:
中的一种,根据图中信息,其结构简式为:
在浓硝酸中放入铜片:
①开始反应的化学方程式为。
②若铜有剩余,则反应将要结束时的反应的离子方程是:
③待反应停止后,再加入少量的25%的稀硫酸,这时铜片上又有气泡产生,其原因是。