已知下热化学方程式:
①H2(g)+1/2O2(g)= H2O(l) ⊿H1= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H2= —241.8kJ/mol
③C(s)+1/2O2 (g) =" CO" (g) ⊿H3= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) ⊿H4= —393.5kJ/mol
回答下列问题:
(1)比较⊿H1, ⊿H2,⊿H3, ⊿H4的大小
(2)上述反应中属于放热的是
(3)H2的燃烧热为 ,C的燃烧热为
(4)燃烧10g H2生成液态水,放出的热量为
(5)CO的燃烧热为 ,其热化学方程式为
(6)分别燃烧1mol C,H2,CO;充分燃烧后它们放出的热量分别为Q1,Q2,Q3
试比较Q1,Q2,Q3的大小
二氧化氯(ClO2)是一种环保型杀菌消毒剂。在生活中主要用于饮用水的消毒和食品保鲜。用二氧化氯消毒后的水可以直接饮用。
二氧化氯是一种黄绿色、有刺激性气味的有毒气体,密度比空气大,其熔点为-59℃,沸点为11.0℃,易溶于水,且与水反应得到酸性溶液。该气体具有强烈的腐蚀性,吸入高浓度二氧化氯气体会引起咳嗽和呼吸道粘膜的损伤。
二氧化氯极其不稳定,受热或见光易发生爆炸性分解,直接造成氯气泄漏而污染环境,所以只有依靠现场制备。工业上用稍潮湿的氯酸钾(KClO3)和草酸(H2C2O4)在60℃时反应制得。由于制取二氧化氯需要使用的氯酸钾是易爆危险品,所以制备和运输成本很高,因此我国目前还未广泛用其消毒自来水。
请依据文章回答下列问题:
(1)本文介绍了二氧化氯的性质、制法和 等方面内容。
(2)二氧化氯的化学性质有① ;② 。
(3)请将制备二氧化氯反应的化学方程式填写完全:
2KClO3 + 2H2C2O4 2ClO2↑+ 2CO2↑ + K2C2O4 +
2ClO2↑+ 2CO2↑ + K2C2O4 +
(4)发生二氧化氯泄漏时,紧急处理方法是 。
A—I是初中化学中常见的物质。它们之间有如下图所示的转化关系。已知A为铝土矿的主要成分,通常情况下F是一种液体,C、D、H、I为气体,H能参与绿色植物的光合作用,G为黑色固体。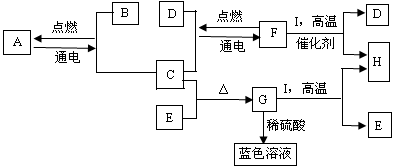
请回答下列问题:
(1)G的化学式是 。
(2)H + 单质碳→I,其反应条件是 。
(3)A 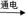 B + C的化学方程式是 。
B + C的化学方程式是 。
(4)I + F(气体) H+D的化学方程式是 。
H+D的化学方程式是 。
现有三瓶失去标签的无色溶液盐酸、氯化钠溶液和澄清石灰水,
(1)往三种无色溶液中加入某种指示剂即可区别它们,该指示剂可选用
(2)装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是
(3)上述溶液中属于盐溶液的是
甲为人体吸入空气和呼出气体成分对比图。CO2含量变化真有这么大?
(1)利用图乙所示 法收集一瓶呼出的气体,标上A;取一个同样装有空气的集气瓶,标上B。将两根同样的小木条点燃后同时伸入A瓶和B瓶,A瓶中的木条先熄灭。这个实验现象 (选填“能”或“不能”)说明呼出的气体中二氧化碳更多。
(2)用大针筒将100ml人体呼出气体压入20ml澄清石灰水中(如图丙),澄清石灰水变浑浊;用同样的方法将100ml空气压入另一瓶20ml澄清石灰水中,请说出澄清石灰水是否变浑浊并解释原因: 。
A.、B、C、D、E、F、G、H、I都是初中化学学过的物质.其中E、F、H均为黑色固体,B为紫红色固体,D为混合物.它们之间有下图转化关系(部分生成物已省去)
(1)指出B的一种用途 ,用化学式表示D的组成 、 .
(2)写出化学方程式:F→E H→C
G→I ,B→H .
(3)上述反应没有涉及到的基本反应类型是