纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2·x H2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用现代分析仪器测定TiO2粒子的大小。用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·x H2O的化学方程式为__________________________。
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是____________;
使用的仪器除天平、药匙、玻璃棒、烧杯、量简外,还需要下图中的_____(填字母代号)。
(3)滴定终点的现象是____________________________________________。
(4)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数表达式为______________________。
(5)判断下列操作对TiO2质量分数测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果_________________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果_____。
葡萄酒中抗氧化剂的残留量是以游离SO2的含量计算,我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。某兴趣小组设计实验方案对葡萄酒中SO2进行测定。
Ⅰ.定性实验方案如下:
(1)将SO2通入水中形成SO2 ─饱和H2SO3溶液体系,此体系中存在多个含硫元素的平衡,分别用平衡方程式表示为_______________。
(2)利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如下实验:
实验结论:干白葡萄酒不能使品红溶液褪色,原因为:_________________________。
Ⅱ.定量实验方案如下(部分装置和操作略):
(3)仪器A的名称是________________。
(4)A中加入100.0mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为______________。
(5)除去B中过量的H2O2,然后再用NaOH标准溶液进行滴定, 除去H2O2的方法是__________。
(6)步骤X滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2的含量为__________g/L。该测定结果比实际值偏高,分析原因________________________。
乙酰苯胺为无色晶体,有“退热冰”之称。其制备原理为:
已知:①苯胺易被氧化;②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
| 试剂名称 |
熔点℃ |
沸点℃ |
溶解度(20 ℃) |
| 苯胺 |
-6.2 |
184.4 |
稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 |
16.7 |
118 |
易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 |
114~116 |
280~290 |
0.46g |
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。
图1图2
(1)仪器a的名称为 。
(2)步骤1中加入锌粉的作用是 。
(3)步骤2中控制温度计示数约105 ℃的原因是 。
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是 ,当过滤的溶液具有强酸性、强碱性或强氧化性时要用 代替布氏漏斗,停止抽滤时的操作为 。
以碳酸镁(含少量FeCO3)为原料制取硫酸镁晶体,并测定Mg2+含量:将原料完全溶于一定量的稀硫酸中,加足量的H2O2后用氨水调节溶液的pH,静置后过滤,除去滤渣,将滤液结晶得硫酸镁晶体。
(1)30.00mL 5.00 mol·L-1的稀硫酸至少能溶解原料的质量为 。
(2)加入H2O2时反应的离子方程式为 。
(3)已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Mg(OH)2]=1.0×10-12。
室温下,若溶液中c(Mg2+)=0.01mol·L-1,欲使溶液中的c(Fe3+)≤1×10-6mol·L-1,需调节溶液pH范围为 。
(4)常采用下列方法测定结晶硫酸镁中Mg2+的含量:
已知:①在pH为9~10时,Mg2+、Zn2+均能与EDTA(H2Y2-)形成配合物
②在pH为5~6时,Zn2+除了与EDTA反应,还能将Mg2+与EDTA形成的配合物中的Mg2+“置换”出来: Zn2+ +MgH2Y=ZnH2Y+Mg2+
步骤1:准确称取得到的硫酸镁晶体1.50g加入过量的EDTA,配成100mL pH在9~10之间溶液A
步骤2:准确移取25.00mL溶液A于锥形瓶中,用0.10mol·L-1Zn2+标准溶液滴定,滴定到终点,消耗Zn2+标准溶液的体积为20.00mL
步骤3:准确移取25.00mL溶液A于另一只锥形瓶中,调节pH在5~6;用0.10mol·L-1Zn2+标准溶液滴定,滴定至终点,消耗Zn2+标准溶液的体积为30.00mL。
计算该结晶硫酸镁中Mg2+的质量分数(请给出计算过程) 。
某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究。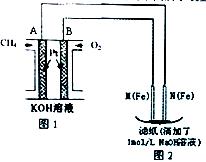

请回答:
Ⅰ.用图1、2所示装置进行第一组实验。
(1)A极发生反应的电极反应式为 。
(2)N极发生反应的电极反应式为 。
(3)滤纸上能观察到的现象有 。
(4)标准状况11.2L CH4反应则图2可收集气体 L(标况)
Ⅱ.用图3所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(5)电解过程中,X极区溶液的pH (填“增大”“减小”或“不变”)。
(6)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-=FeO42-+4H2O和 。
(7)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少 g。
(8)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为 。
一瓶黄色溶液,可能是FeCl3溶液、也可能是碘水、还有可能是久置的浓硝酸(提示:久置的硝酸常因溶有少量NO2而略显黄色)。请设计合理简单的实验探究这瓶黄色溶液的成分。(注意:不考虑以上二种或三种溶液的混合!)
仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙、镊子;氯水、四氯化碳、淀粉溶液、KSCN溶液、铁片、铝片、铜片。(注意:不可另选择仪器和试剂!)
完成以下实验探究过程:
(1)提出假设:
假设1:黄色溶液是FeCl3溶液;
假设2:黄色溶液是碘水;
假设3:黄色溶液是久置的浓硝酸。
(2)设计实验方案
基于假设,设计出实验方案(注意:不用在答题纸上作答)。
(3)实验过程
根据(2)的实验方案,叙述实验操作、预期现象和结论。
【注意】Ⅰ.在答题纸上按以下方式作答,注意前后内容对应;
Ⅱ.注意文字简洁,确保不超出表格。
| 编号 |
实验操作 |
预期现象和结论 |
| ① |
||
| ② |
||
| ③ |