由丙烯经下列反应可得到F、G两种高分子化合物,它们都是常用的塑料。
(1)聚合物F的结构简式是_____________________________________。
(2)D的结构简式是___________________________________________。
(3)B转化为C的化学方程式是_________________________。
(4)在一定条件下,两分子E能脱去两分子水形成一种六元环化合物,该化合物的结构简式是______________________。
(5)E有多种同分异构体,其中一种能发生银镜反应,1mol该种同分异构体与足量的金属钠反应产生1mol H2,则该种同分异构体为__________________________。
下表是元素周期表的一部分,列出了十个元素在周期表中的位置:
| 族 周期 |
IA |
IIA |
IIIA |
VIA |
VA |
VIA |
VIIA |
0 |
| 2 |
⑥ |
⑦ |
||||||
| 3 |
① |
③ |
⑤ |
⑧ |
⑩ |
|||
| 4 |
② |
④ |
⑨ |
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是(填物质化学式),
呈两性的氢氧化物是(填物质化学式);
(3)在⑧与⑨的单质中,氧化性较强的是(填名称)。
(4)用电子式表示元素③与⑧形成化合物的过程。
(5)分别写出⑥元素的氢化物:
a.燃烧的化学方程式,
b.与氯气在光照条件下反应,生成类似甲烷分子结构(正四面体)的氯代烃的化学方程式:。
(6)写出工业冶炼⑤的化学方程式:
(7)上述哪些元素可以从海水中通过一定的方法提取: ,(填元素符号)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的化学方程式; 。
理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+ =2 Ag +Cu2+ ”设制一个化学电池(正极材料用碳棒),回答下列问题:
该电池的电解质溶液是;负极发生反应(填“氧化”或“还原”),电极反应式
有下列各组物质
| A.O2和O3 | B.12C和13C |
C.CH3—CH2—CH2—CH3和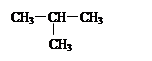 |
|
D. 和 和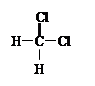 E.甲烷和庚烷 E.甲烷和庚烷 |
(1)_________组两物质互为同位素;(2)__________组两物质互为同素异形体;
(3)_________组两物质属于同系物;(4)_________组两物质互为同分异构体;
工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图所示。反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O===H2SO4+2HI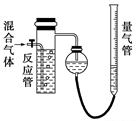
(1)混合气体进入反应管后,量气管内增加的水的体积等于________的体积(填写气体的化学式)。
(2)反应管内溶液蓝色消失后,没有及时停止通气。则测得的SO2含量________(选填“偏高”、“偏低”或“不受影响”)。
(3)反应管内的碘的淀粉溶液也可以用__________代替(填写物质名称)。
(4)若碘溶液体积为Va mL,浓度为c mol·L-1,N2与O2的体积为Vb mL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积百分含量为________。
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为________(选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
工业纯碱主要含有NaCl和NaHCO3杂质,为了鉴定纯碱的含量,常用酸碱滴定测定总碱度,反应产物为NaCl、CO2和H2O。当盐酸与一定工业纯碱恰好完全反应时,溶液pH 3.8~3.9(滴定时NaHCO3也被中和)。工业纯碱的总碱度测定值通常以Na2CO3%和Na2O%表示。
主要实验步骤:①准确称取工业纯碱试样2.00 g;②用适量水配制成体积一定的溶液;③准确移取一定量的所配试液,再用0.01 mol·L-1盐酸标准液滴定,测其总碱度。
请回答以下问题:
(1)称取固体工业纯碱试样时,为什么试样取尽量多些并且力求均匀?
________________________________________________________________________。
(2)在准确称取纯碱试样后,为继续进行实验,除选用烧杯、玻璃棒、酸式滴定管、碱式滴定管、锥形瓶之外。还需要的仪器用品(试剂除外)有
____________________________________________________________。
(3)在滴定操作中,应选用的指示剂是
________________________________________________________________________。
(4)假如所称取的纯碱试样中,除含有2%的NaCl外,另外的杂质中只有NaHCO3,那么NaHCO3含量的大小对该试样总碱度的测定值有何影响?
________________________________________________________________________
________________________________________________________________________。