(10分)实验室用乙醇与浓硫酸共热制取乙烯,常因温度过高生成少量SO2,有人设计了如下图所示实验,以验证上述混合气体中是否含有乙烯和SO2。
⑴.装置中X仪器的名称是: ;碎瓷片的作用是: 。
⑵.写出生成乙烯的反应方程式: 。
⑶.A、B、C、D装置中可盛放的试剂是(从下列所给试剂中选出,填序号):
①品红溶液,②NaOH溶液,③溴水,④KMnO4酸性溶液。
A. ;B. ;C. ;D. 。
⑷.能说明SO2气体存在的现象是 。
⑸.确证含有乙烯的现象是 。
(14分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验: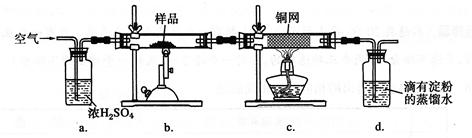

现称取研细的黄铜矿样品1.150 g,在空气存在下进行煅烧,生成Cu、Fe2O3、FeO和SO2气体,实验后取d中溶液的1/10置于锥形瓶中,用0.05000mol·L-1标准碘溶液进行滴定,初读数为0.10 mL,末读数如右图所示。
(1)冶炼铜的反应为8CuFeS2 + 21O2 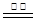 8Cu + 4FeO + 2Fe2O3 + 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
8Cu + 4FeO + 2Fe2O3 + 16SO2,若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
(2)装置a的作用是 。
| A.有利于空气中氧气充分反应 | B.除去空气中的水蒸气 |
| C.有利于气体混合 | D.有利于观察空气流速 |
(3)上述反应结束后,仍需通一段时间的空气,其目的是 。
(4)滴定时,标准碘溶液所耗体积为 mL。用化学方程式表示滴定的原理: 。
(5)通过计算可知,该黄铜矿的纯度为 。
铝是自然界中含量最高的金属元素,以铝土矿(主要成分为Al2O3,还含有Fe2O3)为原料通过以下途径制备氯化铝晶体和绿矾晶体: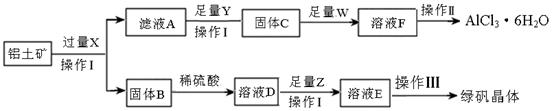
(1)X是__________,操作I是_______。
(2)Z是_____,检验溶液E中含有金属阳离子的实验方法是_______________________。
(3)操作Ⅱ的主要实验步骤是边滴加____(填试剂名称)边蒸发浓缩、冷却结晶、过滤、洗涤。
(4)真空碳热还原—氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g)△H=a kJ·mol-1
3AlCl(g) =2Al(l)+AlCl3(g)△H=b kJ·mol-1
反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H= kJ·mol-1(用含a、b的代数式表示);
(5)铝电池性能优越,海洋灯塔电池是利用铝、石墨为电极材料,海水为电解质溶液,构成电池的其正极反应式为_______________________________;与铅蓄电池相比.释放相同电量时,所消耗金属电极材料的质量比m(Al):m(Pb)=____________。
(6)测定绿矾产品中Fe2+含量的实验步骤:
a.称取5.7g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01mol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40mL(滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
①计算上述产品中FeSO4•7H2O的质量分数为________;
②若用上述方法测定的产品中FeSO4•7H2O的质量分数偏低(测定过程中产生的误差可忽略),其可能原因有___________(只回答一条即可)。
高纯度的单质硅是信息产业的核心资源,没有硅就没有你喜欢的计算机。在地壳中含有大量的硅元素,含量仅次于氧,但自然界中没有游离的硅,硅元素全部是以化合态的形式存在的。工业上主要是利用碳与二氧化硅在高温下反应制备粗硅,某校化学兴趣小组对该反应中气体产物的成分进行探究。
(1)该兴趣小组对气体产物的成分提出如下假设,请你完成假设二和假设三:
假设一:气体产物只有CO;
假设二:____________________;
假设三:_____________________。
……
(2)为探究气体的成分,该兴趣小组设计了如下实验装置: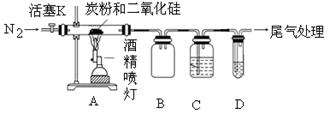
已知:PdCl2溶液可用于检验CO,反应的化学方程式为:CO+PdCl2+H2O=CO2+2HC1 +Pd↓(产生黑色金属钯粉末,使溶液变浑浊);
为避免空气中的氧气、二氧化碳、水蒸气对实验产生干扰,实验时要求通入足够长时间的氮气。
供选试剂:澄清石灰水、PdCl2溶液、浓硫酸、NaOH溶液。
①装置B的作用是______________;
②请你根据上述装置,设计实验验证假设一,写出实验步骤和结论(解答时要求指明C、D中所选试剂的名称):
| 实验步骤(不要求写出具体操作过程) |
实验预期现象和结论 |
(3)有人认为,气体产物的成分与两种反应物的质量之比有关。为了探究炭粉不足时生成物中气体的成分,反应物中炭粉与二氧化硅的质量之比的最大比值是_________。
(4)资料表明,炭粉过量时会生成副产物SiC,若生成物中Si与SiC的物质的量之比为1:2(假定气体产物只有CO),写出该反应的化学方程式:________________________。
氨基甲酸铵是一种用途广泛的化工原料。有关它的资料如下:①常温下,在干燥的空气中稳定,遇水或潮湿空气则生成碳酸铵或碳酸氢铵;②熔点58℃,59℃则可分解成NH3和CO2气体;③在密封管内加热至120℃~140℃时失水生成尿素[CO(NH2)2];④酸性溶液中迅速分解;⑤合成氨基甲酸铵原理为: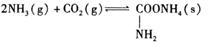
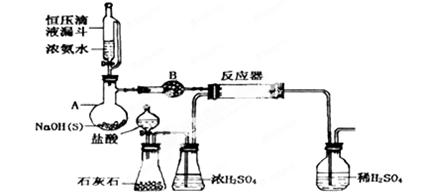
(1)写出氨基甲酸铵在密封管内加热至1200C~1400C生成尿素的反应方程式:_______________
(2)滴液漏斗与容器A相连的导管的作用是 ,容器A内可用 (填药品名称)代替NaOH固体,仪器B名称________;盛放药品是:________。
(3)合成氨基甲酸铵的反应在一定条件下能自发进行,该反应的反应热ΔH_____0(填“>” “=”或“<”)(4)有同学建议该CO2发生装置直接改用“干冰”,你认为他的改进有何优点:(回答二点)
①________________;②________________
(5)该实验装置中有明显导致实验失败的隐患有:(指出主要二处)
①________________;②________________
用石灰石代替碱液处理酸性废水可降低成本。大多数情况下,利用石灰石处理含金属离子的酸性废水并不适用,原因在于酸与石灰石反应的限度,使溶液体系的pH不能达到6.0以上的排放标准。当酸性废水中含有Fe3+、Fe2+、Al3+时能利用石灰石处理该酸性废水,可使pH上升到6.0以上,达到满意效果,其研究步骤如下:
Ⅰ、向0.1mol/L 盐酸,加入石灰石粉,当溶液体系 pH 升至5.6 时, 再继续加入石灰石粉无气泡冒出,说明此时已达溶解平衡。
Ⅱ、向含Fe3+、Fe2+、Al3+的酸性废水中加入适量的0.1mol/L 盐酸和30% H2O2溶液,充分反应。
Ⅲ、将Ⅱ中获得的溶液加入到Ⅰ溶液中,得到混合液x,测得混合液pH<2.0。
Ⅳ、向混合液x中加入石灰石粉,有大量气体产生,并逐渐有沉淀生成。pH 升到 6.2时停止加石灰石粉。
(1)HCl的电子式是 。
(2)石灰石与盐酸反应的离子方程式是 。
(3)从化学平衡的角度分析CaCO3与盐酸反应的原理 (用化学用语表示)。
(4)CaCl2溶液显中性,步骤Ⅰ中溶液体系 pH = 5.6的原因是 。
(5)步骤Ⅱ中反应的离子方程式是 。
(6)已知:生成氢氧化物沉淀的pH
| Al(OH)3 |
Fe(OH)2 |
Fe(OH)3 |
|
| 开始沉淀时 |
3.4 |
6.3 |
1.5 |
| 完全沉淀时 |
4.7 |
8.3 |
2.8 |
注:金属离子的起始浓度为0.1mol/L
根据表中数据解释步骤Ⅱ的目的: 。
(7)步骤Ⅳ中,当 pH 上升到 3.3 以上时,会促进Al3+的水解,Al3+水解的离子方程式是 。
(8)步骤Ⅳ中溶液体系的 pH 可上升到6.2,是因为生成Al(OH)3可与溶液中的HCO3-反应使c(CO32-)增大,该反应的离子方程式是 。